ВИЧ - HIV
| Вирусы иммунодефицита человека | |
|---|---|
 | |
| Сканирующая электронная микрофотография ВИЧ-1 (зеленым цветом), прорастающего из культивированных лимфоцит. Множественные круглые бугорки на поверхности клетки представляют собой места сборки и почкования вирионов. | |
| Научная классификация | |
| (без рейтинга): | Вирус |
| Область: | Рибовирия |
| Королевство: | Парарнавиры |
| Тип: | Artverviricota |
| Учебный класс: | Revtraviricetes |
| Заказ: | Ортервиралес |
| Семья: | Retroviridae |
| Подсемейство: | Orthoretrovirinae |
| Род: | Лентивирус |
| Включенные группы | |
| Другие лентивирусы | |
В вирусы иммунодефицита человека (ВИЧ) два вида Лентивирус (подгруппа ретровирус ), которые заражают людей. Со временем они вызывают синдром приобретенного иммунодефицита (СПИД),[1][2] состояние, при котором прогрессирующий отказ иммунная система позволяет опасно для жизни оппортунистические инфекции и раки процветать.[3] Без лечения средняя продолжительность жизни после заражения ВИЧ составляет от 9 до 11 лет в зависимости от подтипа ВИЧ.[4] В большинстве случаев ВИЧ - это инфекция, передающаяся половым путем и происходит путем контакта или передачи кровь, предэякулят, сперма, и вагинальные жидкости. Исследования показали (как для однополых, так и для разнополых пар), что ВИЧ не передается при половом акте без презерватива, если ВИЧ-положительный партнер имеет неизменно неопределяемую вирусную нагрузку.[5][6] Передача инфекции не половым путем может происходить от инфицированной матери ее младенцу во время беременность, в течение роды контактом с ее кровью или вагинальной жидкостью, а также через грудное молоко.[7][8][9][10] В этих жидкостях организма ВИЧ присутствует как в свободном вирус частицы и вирус внутри инфицированных иммунные клетки.
ВИЧ поражает жизненно важные клетки иммунной системы человека, такие как хелперные Т-клетки (конкретно CD4+ Т-клетки), макрофаги, и дендритные клетки.[11] ВИЧ-инфекция приводит к низкому уровню CD4+ Т-клетки с помощью ряда механизмов, включая пироптоз абортивно инфицированных Т-клеток,[12] апоптоз незараженных клеток-свидетелей,[13] прямое вирусное уничтожение инфицированных клеток и уничтожение инфицированных CD4+ Т-клетки CD8+ цитотоксические лимфоциты распознающие инфицированные клетки.[14] Когда CD4+ Количество Т-клеток снижается ниже критического уровня, клеточный иммунитет теряется, и организм становится все более восприимчивым к оппортунистическим инфекциям, что приводит к развитию СПИДа.
Вирусология
Классификация
| Разновидность | Вирулентность | Инфекционность | Распространенность | Предполагаемое происхождение |
|---|---|---|---|---|
| ВИЧ-1 | Высоко | Высоко | Глобальный | Обыкновенный шимпанзе |
| ВИЧ-2 | Ниже | Низкий | Западная Африка | Закопченный мангабей |
ВИЧ является членом род Лентивирус,[15] часть семьи Retroviridae.[16] У лентивирусов много морфологии и биологический общие свойства. Многие виды заражены лентивирусами, которые, как правило, вызывают длительные заболевания с длительным течением. период инкубации.[17] Лентивирусы передаются как одноцепочечный, положительный-смысл, окутанный РНК-вирусы. При входе в клетку-мишень вирусный РНК геном преобразуется (переписывается) в двухцепочечный ДНК ферментом, кодируемым вирусами, обратная транскриптаза, который транспортируется вместе с вирусным геномом в вирусной частице. Полученная вирусная ДНК затем импортируется в ядро клетки и интегрирован в клеточную ДНК с помощью кодируемого вирусом фермента, интегрировать, и хост кофакторы.[18] После интеграции вирус может стать скрытый, позволяя вирусу и его клетке-хозяину избежать обнаружения иммунной системой в течение неопределенного времени.[19] Вирус ВИЧ может оставаться в спящем состоянии в организме человека до десяти лет после первичного заражения; в этот период вирус не вызывает симптомов. В качестве альтернативы интегрированная вирусная ДНК может быть записано, производя новые геномы РНК и вирусные белки с использованием ресурсов клетки-хозяина, которые упаковываются и высвобождаются из клетки в виде новых вирусных частиц, которые заново начнут цикл репликации.
Были охарактеризованы два типа ВИЧ: ВИЧ-1 и ВИЧ-2. ВИЧ-1 - это вирус, который был первоначально открыт и назван как вирусом, связанным с лимфаденопатией (LAV), так и человеческим Т-лимфотропным вирусом 3 (HTLV-III). ВИЧ-1 больше ядовитый и больше заразный чем ВИЧ-2,[20] и является причиной большинства ВИЧ-инфекций во всем мире. Более низкая инфекционность ВИЧ-2 по сравнению с ВИЧ-1 означает, что меньше людей, подвергшихся воздействию ВИЧ-2, будут инфицированы за один контакт. Из-за своей относительно низкой способности к передаче ВИЧ-2 в основном ограничивается Западная Африка.[21]
Структура и геном

ВИЧ отличается по структуре от других ретровирусов. Он примерно сферический[22] диаметром около 120нм, примерно в 60 раз меньше, чем эритроцит.[23] Он состоит из двух копий позитивных-смысл одноцепочечный РНК что кодирует девять вирусов гены заключен коническим капсид состоит из 2000 копий вирусного белка стр. 24.[24] Одноцепочечная РНК прочно связана с белками нуклеокапсида р7 и ферментами, необходимыми для развития вириона, такими как обратная транскриптаза, протеазы, рибонуклеаза и интегрировать. Матрица, состоящая из вирусного белка p17, окружает капсид, обеспечивая целостность частицы вириона.[24]
Это, в свою очередь, окружено вирусный конверт, который состоит из липидный бислой взятые из мембраны клетки-хозяина человека, когда вновь образовавшаяся вирусная частица выходит из клетки. Вирусная оболочка содержит белки клетки-хозяина и относительно небольшое количество копий белка оболочки ВИЧ,[24] который состоит из крышки, состоящей из трех молекул, известных как гликопротеин (gp) 120, и шток, состоящий из трех gp41 молекулы, которые закрепляют структуру в вирусной оболочке.[25][26] Белок оболочки, кодируемый ВИЧ env ген, позволяет вирусу прикрепляться к клеткам-мишеням и сливать вирусную оболочку с мишенью клеточная мембрана высвобождение вирусного содержимого в клетку и запуск инфекционного цикла.[25]
Как единственный вирусный белок на поверхности вируса, белок оболочки является основной мишенью для Вакцина против ВИЧ усилия.[27] Более половины массы шипа тримерной оболочки связано с N-связью. гликаны. Плотность высока, поскольку гликаны защищают лежащий в основе вирусный белок от нейтрализации антителами. Это одна из известных молекул с наиболее плотным гликозилированием, и ее плотность достаточно высока, чтобы предотвратить нормальный процесс созревания гликанов во время биогенеза в эндоплазматическом аппарате и аппарате Гольджи.[28][29] Таким образом, большинство гликанов застопорились как незрелые гликаны с высоким содержанием маннозы, которые обычно не присутствуют на гликопротеинах человека, которые секретируются или присутствуют на поверхности клетки.[30] Необычный процессинг и высокая плотность означают, что почти все широко нейтрализующие антитела, которые были идентифицированы до сих пор (от подгруппы пациентов, которые были инфицированы в течение многих месяцев или лет), связываются с этими гликанами оболочки или адаптированы для борьбы с ними.[31]
Молекулярная структура вирусного спайка теперь определена Рентгеновская кристаллография[32] и криогенная электронная микроскопия.[33] Эти успехи в структурной биологии стали возможными благодаря развитию стабильных рекомбинантный формы вирусного спайка при введении межсубъединицы дисульфидная связь и изолейцин к пролин мутация (радикальная замена аминокислоты) в gp41.[34] Так называемый SOSIP тримеры не только воспроизводят антигенные свойства нативного вирусного шипа, но также демонстрируют ту же степень незрелости гликанов, что и нативный вирус.[35] Рекомбинантные тримерные вирусные шипы являются многообещающими кандидатами в вакцины, поскольку обладают меньшим количеством не нейтрализующих эпитопы чем рекомбинантный мономерный gp120, который подавляет иммунный ответ на целевые эпитопы.[36]

Геном РНК состоит как минимум из семи структурных ориентиров (LTR, ТАР, RRE, PE, SLIP, CRS и INS) и девять генов (кляп, pol, и env, тат, rev, неф, vif, впр, впу, а иногда и десятый tev, который представляет собой сплав тат, env и rev), кодирующий 19 белков. Три из этих генов, кляп, pol, и env, содержат информацию, необходимую для создания структурных белков для новых вирусных частиц.[24] Например, env кодирует белок gp160, который клеточной протеазой разрезает пополам с образованием gp120 и gp41. Шесть оставшихся генов, тат, rev, неф, vif, впр, и впу (или же vpx в случае ВИЧ-2) - это регуляторные гены белков, которые контролируют способность ВИЧ инфицировать клетки, производить новые копии вируса (реплицироваться) или вызывать заболевание.[24]
Два тат белки (p16 и p14) являются транскрипционные трансактиваторы для LTR промоутер действуя путем связывания элемента РНК TAR. TAR также может быть преобразован в микроРНК которые регулируют апоптоз гены ERCC1 и IER3.[37][38] В rev белок (p19) участвует в перемещении РНК из ядра и цитоплазмы, связываясь с RRE Элемент РНК. В vif белок (p23) предотвращает действие APOBEC3G (клеточный белок, дезаминирует цитидин к уридин в одноцепочечной вирусной ДНК и / или препятствует обратной транскрипции[39]). В впр белок (p14) задерживает деление клеток в G2 / M. В неф белок (p27) подавляет CD4 (главный вирусный рецептор), а также MHC класс I и класс II молекулы.[40][41][42]
Неф также взаимодействует с SH3 домены. В впу белок (p16) влияет на высвобождение новых вирусных частиц из инфицированных клеток.[24] Концы каждой цепи РНК ВИЧ содержат последовательность РНК, называемую длинный терминальный повтор (LTR). Области в LTR действуют как переключатели для контроля производства новых вирусов и могут запускаться белками либо из ВИЧ, либо из клетки-хозяина. В Пси элемент участвует в упаковке вирусного генома и распознается кляп и rev белки. Элемент SLIP (TTTTTT) участвует в сдвиг рамки в кляп-pol рамка чтения необходимо сделать функциональным pol.[24]
Тропизм

Период, термин вирусный тропизм относится к типам клеток, которые заражает вирус. ВИЧ может инфицировать различные иммунные клетки, такие как CD4+ Т-клетки, макрофаги, и микроглиальные клетки. Поступление ВИЧ-1 в макрофаги и CD4+ Т-клетки опосредуются посредством взаимодействия гликопротеинов оболочки вириона (gp120) с молекулой CD4 на мембране клеток-мишеней, а также с хемокин корецепторы.[25][43]
Макрофаготропные (М-тропные) штаммы ВИЧ-1 или не-синцития -индуцирующие штаммы (NSI; теперь называемые вирусом R5[44]) использовать β-хемокиновый рецептор, CCR5, для входа и, таким образом, способны реплицироваться как в макрофагах, так и в CD4+ Т-клетки.[45] Этот корецептор CCR5 используется почти всеми первичными изолятами ВИЧ-1 независимо от генетического подтипа вируса. Действительно, макрофаги играют ключевую роль в нескольких важных аспектах ВИЧ-инфекции. Они кажутся первыми клетками, инфицированными ВИЧ, и, возможно, источником продукции ВИЧ, когда CD4+ клетки у пациента истощаются. Макрофаги и микроглиальные клетки - это клетки, инфицированные ВИЧ в Центральная нервная система. в миндалины и аденоиды у ВИЧ-инфицированных макрофаги сливаются в многоядерные гигантские клетки которые производят огромное количество вирусов.
Т-тропные штаммы ВИЧ-1, или синцития -индуцирующие штаммы (SI; теперь называемые вирусами X4[44]) реплицируются в первичном CD4+ Т-клетки, а также в макрофагах и используют α-хемокиновый рецептор, CXCR4, для входа.[45][46][47]
Считается, что двухтропные штаммы ВИЧ-1 являются переходными штаммами ВИЧ-1 и, таким образом, могут использовать как CCR5, так и CXCR4 в качестве корецепторов для проникновения вируса.
В α-хемокин SDF-1, а лиганд для CXCR4 подавляет репликацию Т-тропных изолятов ВИЧ-1. Он делает это понижающий экспрессия CXCR4 на поверхности клеток-мишеней ВИЧ. Изоляты M-тропного ВИЧ-1, в которых используется только рецептор CCR5, обозначаются R5; те, которые используют только CXCR4, называются X4, а те, которые используют оба, X4R5. Однако использование только корецепторов не объясняет вирусный тропизм, поскольку не все вирусы R5 могут использовать CCR5 на макрофагах для продуктивной инфекции.[45] и ВИЧ также может инфицировать подтип миелоидные дендритные клетки,[48] которые, вероятно, составляют резервуар который поддерживает инфекцию, когда CD4+ Количество Т-клеток снизилось до чрезвычайно низкого уровня.
Некоторые люди устойчивы к определенным штаммам ВИЧ.[49] Например, люди с CCR5-Δ32 мутации устойчивы к заражению вирусом R5, так как мутация не позволяет ВИЧ связываться с этим корецептором, что снижает его способность инфицировать клетки-мишени.
Половой акт это основной путь передачи ВИЧ. И X4, и R5 HIV присутствуют в семенная жидкость, что позволяет вирусу передаваться от мужчины к его сексуальный партнер. Затем вирионы могут инфицировать многочисленные клеточные мишени и распространяться по всему организму. Однако процесс отбора[требуется дальнейшее объяснение ] приводит к преимущественной передаче вируса R5 по этому пути.[50][51][52] У пациентов, инфицированных ВИЧ-1 подтипа B, часто наблюдается переключение корецепторов на поздних стадиях заболевания и Т-тропные варианты, которые могут инфицировать различные Т-клетки через CXCR4.[53] Затем эти варианты реплицируются более агрессивно с повышенной вирулентностью, что вызывает быстрое истощение Т-клеток, коллапс иммунной системы и оппортунистические инфекции, знаменующие появление СПИДа.[54] ВИЧ-инфицированные пациенты заражаются чрезвычайно широким спектром оппортунистических инфекций, что было особенно проблематично до начала заболевания. ВААРТ терапии; тем не менее, те же самые инфекции регистрируются среди ВИЧ-инфицированных пациентов, обследованных после смерти после начала антиретровирусной терапии.[3] Таким образом, в ходе инфекции адаптация вируса к использованию CXCR4 вместо CCR5 может быть ключевым этапом в прогрессировании СПИДа. Ряд исследований с участием людей, инфицированных подтипом B, показал, что от 40 до 50 процентов пациентов со СПИДом могут быть носителями вирусов SI и, как предполагается, фенотипа X4.[55][56]
ВИЧ-2 гораздо менее патогенен, чем ВИЧ-1, и его распространение во всем мире ограничивается Западная Африка. Принятие «дополнительных генов» ВИЧ-2 и его другими беспорядочный Модель использования корецепторов (включая независимость от CD4) может помочь вирусу в его адаптации, чтобы избежать врожденных факторов рестрикции, присутствующих в клетках-хозяевах. Адаптация к использованию нормальных клеточных механизмов для передачи и продуктивной инфекции также способствовала репликации ВИЧ-2 у людей. Стратегия выживания любого инфекционного агента состоит не в том, чтобы убить своего хозяина, а в том, чтобы в конечном итоге стать комменсальный организм. Достигнув низкой патогенности, со временем будут отобраны варианты, которые более успешны при передаче.[57]
Цикл репликации
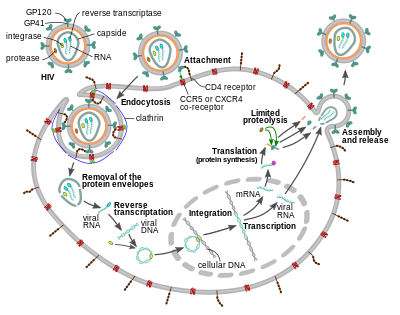
Вход в камеру

Вирион ВИЧ попадает макрофаги и CD4+ Т-клетки посредством адсорбция из гликопротеины на его поверхности к рецепторам на клетке-мишени с последующим слиянием вирусный конверт с мембраной клетки-мишени и высвобождением капсида ВИЧ в клетку.[58][59]
Вход в клетку начинается через взаимодействие комплекса тримерной оболочки (gp160 спайк) на вирусной оболочке ВИЧ и обоих CD4 и корецептор хемокина (обычно либо CCR5 или же CXCR4, но другие, как известно, взаимодействуют) на поверхности клетки-мишени.[58][59] Gp120 связывается с интегрин α4β7 активация LFA-1, центральный интегрин, участвующий в создании вирусологические синапсы, которые способствуют эффективному распространению ВИЧ-1 от клетки к клетке.[60] Спайк gp160 содержит связывающие домены как для рецепторов CD4, так и для хемокинов.[58][59]
Первый шаг в слиянии включает высокоаффинное присоединение CD4-связывающих доменов gp120 к CD4. Как только gp120 связывается с белком CD4, комплекс оболочки претерпевает структурные изменения, обнажая связывающие домены хемокинового рецептора gp120 и позволяя им взаимодействовать с целевым хемокиновым рецептором.[58][59] Это обеспечивает более стабильное двустороннее крепление, что позволяет N-концевой слитый пептид gp41 для проникновения через клеточную мембрану.[58][59] Повторить последовательности в gp41, HR1 и HR2 затем взаимодействуют, вызывая коллапс внеклеточной части gp41 в форму шпильки. Эта петлевая структура сближает вирус и клеточные мембраны, обеспечивая слияние мембран и последующее проникновение вирусного капсида.[58][59]
После связывания ВИЧ с клеткой-мишенью в клетку вводятся РНК ВИЧ и различные ферменты, включая обратную транскриптазу, интегразу, рибонуклеазу и протеазу.[58][неудачная проверка ] Вовремя микротрубочка На основе транспорта в ядро вирусный геном с одноцепочечной РНК транскрибируется в двухцепочечную ДНК, которая затем интегрируется в хромосому хозяина.
ВИЧ может заразить дендритные клетки (DC) этим маршрутом CD4-CCR5, но другим маршрутом, использующим маннозо-специфические рецепторы лектина С-типа Такие как DC-SIGN также можно использовать.[61] ДК - одни из первых клеток, с которыми вирус сталкивается при передаче половым путем. В настоящее время считается, что они играют важную роль, передавая ВИЧ Т-лимфоцитам, когда вирус захватывается в слизистая оболочка DC.[61] Наличие СЭЗ-1, что естественно встречается в нейроны, как полагают, предотвращает инфицирование клеток ВИЧ.[62]
Долгое время считалось, что проникновение ВИЧ-1, как и проникновение многих других ретровирусов, происходит исключительно через плазматическую мембрану. Однако в последнее время продуктивное заражение pH -независимый, клатрин-опосредованный эндоцитоз также сообщалось о ВИЧ-1, и недавно было предложено, что это единственный путь продуктивного проникновения.[63][64][65][66][67]
Репликация и транскрипция
Вскоре после того, как вирусный капсид попадает в клетку, фермент называется обратная транскриптаза освобождает одноцепочечный позитивный смысл РНК геном из прикрепленных вирусных белков и копирует его в комплементарная ДНК (кДНК) молекула.[68] Процесс обратной транскрипции чрезвычайно подвержен ошибкам, и возникающие в результате мутации могут вызывать устойчивость к лекарству или позволить вирусу ускользнуть от иммунной системы организма. Обратная транскриптаза также обладает рибонуклеазной активностью, которая разрушает вирусную РНК во время синтеза кДНК, а также ДНК-зависимой активностью ДНК-полимеразы, которая создает смысл ДНК из антисмысловой кДНК.[69] Вместе кДНК и ее комплемент образуют двухцепочечную вирусную ДНК, которая затем транспортируется в ядро клетки. Интеграция вирусной ДНК в клетки-хозяева геном осуществляется другим вирусным ферментом, называемым интегрировать.[68]
Интегрированная вирусная ДНК может тогда находиться в спящем состоянии на латентной стадии ВИЧ-инфекции.[68] Чтобы активно продуцировать вирус, определенные клеточные факторы транскрипции должны присутствовать, наиболее важным из которых является NF-κB (ядерный фактор каппа B), который активируется при активации Т-клеток.[70] Это означает, что клетки, которые, скорее всего, станут мишенью, проникнуты и впоследствии убиты ВИЧ, будут активно бороться с инфекцией.
Во время репликации вируса интегрированная ДНК провирус является записано в РНК, некоторые из которых затем подвергаются Сплайсинг РНК производить зрелые информационные РНК (мРНК). Эти мРНК экспортируются из ядра в цитоплазма, где они переведено в регуляторные белки Tat (что стимулирует производство новых вирусов) и Rev. По мере того, как продуцируется только что продуцируемый белок Rev, он перемещается в ядро, где связывается с полноразмерными, несплицированными копиями вирусных РНК и позволяет им покинуть ядро.[71] Некоторые из этих полноразмерных РНК функционируют как новые копии вирусного генома, тогда как другие функционируют как мРНК, которые транслируются с образованием структурных белков Gag и Env. Белки Gag связываются с копиями генома вирусной РНК, упаковывая их в новые вирусные частицы.[72]
ВИЧ-1 и ВИЧ-2, по-видимому, по-разному упаковывают свою РНК.[73][74] ВИЧ-1 будет связываться с любой подходящей РНК.[75] ВИЧ-2 будет предпочтительно связываться с мРНК, которая использовалась для создания самого белка Gag.[76]
Рекомбинация
В каждой частице ВИЧ-1 заключены два генома РНК (см. Структура и геном ВИЧ ). При инфицировании и репликации, катализируемых обратной транскриптазой, может происходить рекомбинация между двумя геномами.[77][78] Рекомбинация происходит, когда одноцепочечные геномы с положительной РНК подвергаются обратной транскрипции с образованием ДНК. Во время обратной транскрипции формирующаяся ДНК может многократно переключаться между двумя копиями вирусной РНК. Эта форма рекомбинации известна как выбор копии. События рекомбинации могут происходить по всему геному. В каждом цикле репликации может происходить от двух до 20 событий рекомбинации на геном, и эти события могут быстро перетасовать генетическую информацию, которая передается от родительских геномов к потомкам.[78]
Вирусная рекомбинация вызывает генетические вариации, которые, вероятно, вносят вклад в эволюция сопротивления антиретровирусная терапия.[79] В принципе рекомбинация также может способствовать преодолению иммунной защиты хозяина. Тем не менее, для реализации адаптивных преимуществ генетической изменчивости, два вирусных генома, упакованные в отдельные вирусные частицы, должны возникать из отдельных родительских родительских вирусов с разной генетической структурой. Неизвестно, как часто такая смешанная упаковка встречается в естественных условиях.[80]
Bonhoeffer и другие.[81] предположили, что переключение матрицы с помощью обратной транскриптазы действует как процесс репарации для устранения разрывов в геноме одноцепочечной РНК. Кроме того, Ху и Темин[77] предположили, что рекомбинация является адаптацией для восстановления повреждений в геномах РНК. Переключение цепи (рекомбинация с выбором копии) с помощью обратной транскриптазы может генерировать неповрежденную копию геномной ДНК из двух поврежденных копий генома одноцепочечной РНК. Такой взгляд на адаптивное преимущество рекомбинации при ВИЧ может объяснить, почему каждая частица ВИЧ содержит два полных генома, а не один. Более того, точка зрения, что рекомбинация - это процесс репарации, подразумевает, что польза от репарации может проявляться в каждом цикле репликации, и что это преимущество может быть реализовано независимо от того, отличаются ли два генома генетически. С точки зрения того, что рекомбинация при ВИЧ является процессом репарации, генерация рекомбинационной вариации будет следствием, но не причиной эволюции переключения матрицы.[81]
Причины заражения ВИЧ-1 хроническое воспаление и производство активные формы кислорода.[82] Таким образом, геном ВИЧ может быть уязвим для окислительные повреждения, включая разрывы в одноцепочечной РНК. Для ВИЧ, как и для вирусов в целом, успешное инфицирование зависит от преодоления защитных стратегий хозяина, которые часто включают производство активных форм кислорода, повреждающих геном. Таким образом, Мичод и другие.[83] предположили, что рекомбинация с помощью вирусов является адаптацией для восстановления повреждений генома, а рекомбинационная вариация - побочным продуктом, который может дать отдельную пользу.
Сборка и выпуск
Заключительный этап вирусного цикла - сборка новых вирионов ВИЧ-1 - начинается с плазматическая мембрана клетки-хозяина. Полипротеин Env (gp160) проходит через эндоплазматический ретикулум и транспортируется в аппарат Гольджи где это расколотый к фурин в результате образуются два гликопротеина оболочки ВИЧ, gp41 и gp120.[84] Они транспортируются к плазматической мембране клетки-хозяина, где gp41 закрепляет gp120 на мембране инфицированной клетки. Полипротеины Gag (p55) и Gag-Pol (p160) также связываются с внутренней поверхностью плазматической мембраны вместе с геномной РНК ВИЧ, когда формирующийся вирион начинает отрастать от клетки-хозяина. Бутонизированный вирион еще незрел, поскольку кляп полипротеины все еще необходимо расщепить на белки матрикса, капсида и нуклеокапсида. Это расщепление опосредуется упакованной вирусной протеазой и может ингибироваться антиретровирусными препаратами ингибитор протеазы учебный класс. Затем различные структурные компоненты собираются, чтобы произвести зрелый вирион ВИЧ.[85] Тогда только зрелые вирионы могут инфицировать другую клетку.
Распространение по телу

Классический процесс заражения клетки вирионом можно назвать «бесклеточным распространением», чтобы отличить его от недавно признанного процесса, называемого «межклеточное распространение».[86] При бесклеточном распространении (см. Рисунок) вирусные частицы отталкиваются от инфицированной Т-клетки, попадают в кровь или внеклеточной жидкости а затем заразить другую Т-клетку после случайной встречи.[86] ВИЧ также может распространяться путем прямой передачи от одной клетки к другой в процессе распространения от клетки к клетке, для чего были описаны два пути. Во-первых, инфицированная Т-клетка может передавать вирус непосредственно целевой Т-клетке через вирусологический синапс.[60][87] Во-вторых, антигенпрезентирующая клетка (APC), такие как макрофаг или дендритная клетка, могут передавать ВИЧ к Т-клеткам посредством процесса, который включает либо продуктивную инфекцию (в случае макрофагов), либо захват и перенос вирионов в транс (в случае дендритных клеток).[88] Какой бы путь ни использовался, сообщается, что инфицирование путем передачи вируса от клетки к клетке намного эффективнее, чем распространение вируса вне клетки.[89] Этой повышенной эффективности способствует ряд факторов, в том числе отпочкование поляризованного вируса к месту межклеточного контакта, близкое расположение клеток, что минимизирует жидкую фазу. распространение вирионов и скопление рецепторов входа ВИЧ на клетке-мишени в направлении зоны контакта.[87] Считается, что распространение от клетки к клетке особенно важно в лимфоидные ткани где CD4+ Т-клетки плотно упакованы и могут часто взаимодействовать.[86] Исследования прижизненной визуализации подтвердили концепцию вирусологического синапса ВИЧ. in vivo.[90] Многие механизмы распространения, доступные для ВИЧ, способствуют продолжающейся репликации вируса, несмотря на антиретровирусную терапию.[86][91]
Генетическая изменчивость

ВИЧ отличается от многих вирусов тем, что имеет очень высокую генетическая изменчивость. Это разнообразие - результат быстрого цикл репликации, с генерацией около 1010 вирионы каждый день в сочетании с высоким скорость мутации примерно 3 х 10−5 на нуклеотидное основание за цикл репликации и рекомбиногенный свойства обратной транскриптазы.[92][93][94]
Этот сложный сценарий приводит к появлению множества вариантов ВИЧ у одного инфицированного пациента в течение одного дня.[92] Эта вариабельность усугубляется, когда одна клетка одновременно заражается двумя или более разными штаммами ВИЧ. Когда одновременное заражение происходит, геном потомства вирионов может состоять из цепей РНК от двух разных штаммов. Затем этот гибридный вирион заражает новую клетку, где подвергается репликации. Когда это происходит, обратная транскриптаза, перепрыгивая между двумя разными шаблонами РНК, будет генерировать вновь синтезированный ретровирус. Последовательность ДНК это рекомбинант между двумя родительскими геномами.[92] Эта рекомбинация наиболее очевидна, когда она происходит между подтипами.[92]
Тесно связанные вирус обезьяньего иммунодефицита (SIV) превратился во множество штаммов, классифицированных по естественным видам хозяев. SIV штаммы Африканская зеленая обезьяна (SIVagm) и закопченный мангабей Считается, что (SIVsmm) имеют долгую историю эволюции со своими хозяевами. Эти хозяева адаптировались к присутствию вируса,[95] который присутствует в больших количествах в крови хозяина, но вызывает только слабый иммунный ответ,[96] не вызывает развития обезьяньего СПИДа,[97] и не подвергается обширным мутациям и рекомбинации, типичным для ВИЧ-инфекции у людей.[98]
Напротив, когда эти штаммы заражают виды, которые не адаптировались к SIV («гетерологичные» или похожие хозяева, такие как резус или же циномологи макаки ), у животных развивается СПИД, и вирус вызывает генетическое разнообразие аналогично тому, что наблюдается при ВИЧ-инфекции у человека.[99] Шимпанзе SIV (SIVcpz), ближайший генетический родственник ВИЧ-1, связан с повышенной смертностью и СПИД-подобными симптомами у его естественного хозяина.[100] SIVcpz, по-видимому, относительно недавно был передан популяциям шимпанзе и людей, поэтому их хозяева еще не адаптировались к вирусу.[95] Этот вирус также потерял функцию неф ген, который присутствует в большинстве SIV. Для непатогенных вариантов SIV, неф подавляет активацию Т-лимфоцитов через CD3 маркер. НефФункция при непатогенных формах ВИО заключается в подавлять выражение воспалительные цитокины, MHC-1 и сигналы, влияющие на трафик Т-клеток. При ВИЧ-1 и SIVcpz, неф не подавляет активацию Т-клеток и утратил эту функцию. Без этой функции более вероятно истощение Т-лимфоцитов, что приведет к иммунодефициту.[100][101]
Три группы ВИЧ-1 были идентифицированы на основе различий в оболочке (env) регион: M, N и O.[102] Группа M является наиболее распространенной и подразделяется на восемь подтипов (или клады ), основанные на целом геноме, которые географически различны.[103] Наиболее распространены подтипы B (в основном в Северной Америке и Европе), A и D (в основном в Африке) и C (в основном в Африке и Азии); эти подтипы образуют ветви в филогенетическое дерево представляющий происхождение группы M ВИЧ-1. Коинфекция с различными подтипами дает начало циркулирующим рекомбинантным формам (CRF). В 2000 году, последнем году, в котором был проведен анализ глобальной распространенности подтипа, 47,2% инфекций во всем мире относились к подтипу C, 26,7% - к подтипу A / CRF02_AG, 12,3% - к подтипу B, 5,3% - к подтипу D, 3,2% относились к CRF_AE, а остальные 5,3% составляли другие подтипы и CRF.[104] Большинство исследований ВИЧ-1 сосредоточено на подтипе B; немногие лаборатории специализируются на других подтипах.[105] Существование четвертой группы, «P», было выдвинуто на основании вируса, изолированного в 2009 году.[106] Штамм, по-видимому, происходит от горилла SIV (SIVgor), впервые выделенный из западные равнинные гориллы в 2006 году.[106]
Ближайшим родственником ВИЧ-2 является SIVsm, штамм SIV, обнаруженный в сажистых мангабах. Поскольку ВИЧ-1 происходит от SIVcpz, а ВИЧ-2 - от SIVsm, генетическая последовательность ВИЧ-2 лишь частично гомологична ВИЧ-1 и больше напоминает последовательность SIVsm.[нужна цитата ][107]
Диагностика
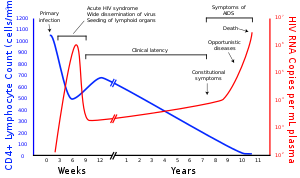
Многие ВИЧ-положительные люди не знают, что они инфицированы вирусом.[108] Например, в 2001 году менее 1% сексуально активного городского населения в Африке прошли тестирование, а в сельской местности эта доля еще ниже.[108] Кроме того, в 2001 г. только 0,5% беременные женщины посещающие городские медицинские учреждения были проконсультированы, протестированы или получили их результаты.[108] Опять же, в сельских медицинских учреждениях эта доля еще ниже.[108] Поскольку доноры могут не знать о своей инфекции, донорская кровь и продукты крови, используемые в медицине и медицинские исследования регулярно проходят скрининг на ВИЧ.[109]
Первоначально тестирование на ВИЧ-1 проводится с использованием иммуноферментный анализ (ИФА) для выявления антител к ВИЧ-1. Образцы с нереактивным результатом первоначального ИФА считаются ВИЧ-отрицательными, если только не произошел новый контакт с инфицированным партнером или партнером с неизвестным ВИЧ-статусом. Образцы с реактивным результатом ELISA повторно тестируются в двух экземплярах.[110] Если результат любого повторного теста является реактивным, образец регистрируется как повторно реактивный и подвергается подтверждающему тестированию с помощью более конкретного дополнительного теста (например, полимеразной цепной реакции (ПЦР), вестерн-блот или, реже, иммунофлуоресцентный анализ (ЕСЛИ)). Только образцы, которые являются повторно реактивными по данным ELISA и положительными по данным IFA или ПЦР или реактивными по данным вестерн-блоттинга, считаются ВИЧ-положительными и указывают на ВИЧ-инфекцию. Образцы, которые повторно реагируют на ELISA, иногда дают неопределенный результат вестерн-блоттинга, который может быть либо неполным ответом антител на ВИЧ у инфицированного человека, либо неспецифическими реакциями у неинфицированного человека.[111]
Хотя ИФА можно использовать для подтверждения инфекции в этих неоднозначных случаях, этот анализ не получил широкого распространения. Как правило, второй образец следует собирать более чем через месяц и повторно тестировать для лиц с неопределенными результатами вестерн-блоттинга. Хотя гораздо реже доступны, тестирование нуклеиновой кислоты (например, метод амплификации вирусной РНК или провирусной ДНК) также может помочь в диагностике в определенных ситуациях.[110] Кроме того, несколько протестированных образцов могут дать неубедительные результаты из-за малого количества образцов. В этих ситуациях берется второй образец и тестируется на ВИЧ-инфекцию.
Современное тестирование на ВИЧ является чрезвычайно точным, когда период окна принимается во внимание. Один скрининговый тест является правильным более чем в 99% случаев.[113] Вероятность ложноположительного результата в стандартном двухэтапном протоколе тестирования оценивается примерно в 1 из 250 000 в популяции с низким уровнем риска.[114] Тестирование после контакта рекомендуется немедленно, а затем через шесть недель, три месяца и шесть месяцев.[115]
Последние рекомендации США Центры по контролю и профилактике заболеваний (CDC) показывают, что тестирование на ВИЧ должно начинаться с иммуноанализ комбинированный тест на ВИЧ-1 и ВИЧ-2 антитела и p24 антиген. Отрицательный результат исключает контакт с ВИЧ, в то время как положительный результат должен сопровождаться иммуноанализом на дифференцировку антител к ВИЧ-1/2, чтобы определить, какие антитела присутствуют. Это дает четыре возможных сценария:
- 1. ВИЧ-1 (+) и ВИЧ-2 (-): обнаружены антитела к ВИЧ-1.
- 2. ВИЧ-1 (-) и ВИЧ-2 (+): обнаружены антитела к ВИЧ-2.
- 3. ВИЧ-1 (+) и ВИЧ-2 (+): обнаружены антитела к ВИЧ-1 и ВИЧ-2.
- 4. ВИЧ-1 (-) или неопределенный и ВИЧ-2 (-): Тест на нуклеиновую кислоту необходимо проводить для выявления острой инфекции ВИЧ-1 или ее отсутствия.[116]
Исследование
Исследования ВИЧ / СПИДа включают все медицинские исследования который пытается предотвратить, лечить или вылечить ВИЧ / СПИД, а также фундаментальные исследования о природе ВИЧ как инфекционного агента и СПИДа как болезни, вызываемой ВИЧ.
Многие правительства и исследовательские учреждения участвуют в исследованиях по ВИЧ / СПИДу. Это исследование включает поведенческие медицинские вмешательства, например, исследование половое воспитание, и разработка лекарств, например, исследование микробициды от болезней, передающихся половым путем, Вакцины против ВИЧ, и антиретровирусные препараты.[117] Другие области медицинских исследований включают темы предэкспозиционная профилактика, постконтактная профилактика, обрезание и ВИЧ, и эффекты ускоренного старения.
Лечение и передача
Лечение ВИЧ / СПИДа обычно включает в себя использование нескольких антиретровирусные препараты. Во многих частях мира ВИЧ превратился в хроническое заболевание, при котором прогрессирует СПИД встречается все реже.
Латентный период ВИЧ и, как следствие, вирусный резервуар CD4+ Т-клетки, дендритные клетки, а также макрофаги являются основным препятствием на пути уничтожения вируса.[19]
Важно отметить, что, хотя ВИЧ очень вирулентен, передача не происходит половым путем, если у ВИЧ-инфицированного человека неизменно неопределяется вирусная нагрузка (<50 копий / мл) из-за антиретровирусного лечения. Ранее было сказано, что вероятность передачи «очень низкая» или «ничтожная» («Заявление Швейцарии»).[118] Однако после многочисленных исследований стало ясно, что вероятность передачи ВИЧ половым путем фактически равна нулю, если у ВИЧ-положительного человека вирусная нагрузка неизменно не определяется; это известно как U = U, «Undetectable = Untransmittable», также выражается как «не могу передать это».[119][120] Исследования, демонстрирующие U = U: Противоположности притягиваются,[121] ПАРТНЕР 1,[122] ПАРТНЕР 2,[5][123] (для пар мужчина-мужчина)[124] и HPTN052[125] (для гетеросексуальных пар), когда «партнер, живущий с ВИЧ, имел длительно подавленную вирусную нагрузку».[124] В этих исследованиях принимали участие пары, в которых один партнер был ВИЧ-положительным, а другой - отрицательным, и проходили регулярное тестирование на ВИЧ. Всего по четырем исследованиям было зарегистрировано 4097 пар на четырех континентах, и было зарегистрировано 151 880 половых актов без презерватива; не было ни одной филогенетически связанной передачи ВИЧ, когда у положительного партнера вирусная нагрузка не определялась.[126] После этого заявление о консенсусе U = U, поддерживающее использование «нулевого риска», было подписано сотнями людей и организаций, включая США. CDC, Британская ассоциация по ВИЧ и Ланцет медицинский журнал.[127] Важность окончательных результатов исследования PARTNER 2 описал медицинский директор Терренс Хиггинс Trust как «невозможно переоценить», в то время как ведущий автор Элисон Роджер заявила, что сообщение о том, что «неопределяемая вирусная нагрузка делает ВИЧ непередаваемым ... может помочь положить конец пандемии ВИЧ, предотвратив передачу ВИЧ.[128] Авторы обобщили свои выводы в Ланцет следующее:[5]
Наши результаты обеспечивают уровень доказательств подавления вируса и риска передачи ВИЧ для геев, аналогичный тому, который ранее был получен для гетеросексуальных пар, и предполагают, что риск передачи ВИЧ в однополых парах через секс без презерватива при подавлении вирусной нагрузки ВИЧ фактически равен нулю. Наши результаты подтверждают идею кампании U = U (необнаружимое равно непередаваемое) и преимущества раннего тестирования и лечения ВИЧ.[5]
Этот результат согласуется с выводом, представленным Энтони С. Фаучи, директор Национальный институт аллергии и инфекционных заболеваний для США Национальные институты здоровья, и его команда в точке зрения, опубликованной в Журнал Американской медицинской ассоциации, что U = U - эффективный метод профилактики ВИЧ, когда сохраняется неопределяемая вирусная нагрузка.[6][124]
Генитальный герпес Реактивация (HSV-2) у инфицированных вирусом приводит к увеличению количества CD4 + T-клеток, обогащенных CCR-5, а также воспалительных дендритных клеток в подслизистой оболочке кожи половых органов. Тропизм ВИЧ к CCR-5-позитивным клеткам объясняет двух-трехкратное увеличение заражения ВИЧ среди людей с генитальным герпесом. Ежедневное лечение противовирусными препаратами (например, ацикловиром) не снижает субклиническое постреактивационное воспаление и, следовательно, не снижает риск заражения ВИЧ.[129][130]
История
Открытие
Первая новость о "новой экзотической болезни" появилась 18 мая 1981 года в газете для геев. Уроженец Нью-Йорка.[131]
СПИД был впервые клинически обнаружен в 1981 году в США.[132] Первоначальные случаи были группой потребителей инъекционных наркотиков и геев без известной причины нарушения иммунитета, которые проявляли симптомы Пневмоцисты пневмония (PCP или PJP, последний термин означает, что возбудитель теперь называется Pneumocystis jirovecii), редкой оппортунистической инфекции, которая, как известно, возникает у людей с очень ослабленной иммунной системой.[133] Вскоре после этого у других мужчин-геев развился ранее редкий рак кожи под названием Саркома Капоши (KS).[134][135] Возникло еще много случаев PJP и KS, что насторожило США. Центры по контролю и профилактике заболеваний (CDC) и целевая группа CDC была сформирована для мониторинга вспышки.[136] Считается, что самый ранний ретроспективно описанный случай СПИДа произошел в Норвегии в 1966 году.[137]
Вначале CDC не имел официального названия болезни, часто ссылаясь на нее через болезни, которые были с ней связаны, например, лимфаденопатия болезнь, в честь которой первооткрыватели ВИЧ назвали вирус.[138][139] Они также использовали Саркома Капоши и оппортунистические инфекции, название, под которым целевая группа была создана в 1981 году.[140] В общей прессе термин СЕТКА, который обозначал иммунодефицит, связанный с геями, был придуман.[141] CDC в поисках названия и изучении зараженных сообществ придумал «болезнь 4H», поскольку, казалось, выделял гомосексуалистов, потребителей героина, больные гемофилией, и Гаитяне.[142][143] Однако после определения того, что СПИД не был изолирован от гей-сообщество,[140] стало ясно, что термин GRID вводит в заблуждение и СПИД был представлен на собрании в июле 1982 г.[144] К сентябрю 1982 года CDC начал использовать название СПИД.[145]

В 1983 году две отдельные исследовательские группы под руководством американского Роберт Галло и французские следователи Франсуаза Барре-Синусси и Люк Монтанье независимо заявили, что новый ретровирус мог заразить больных СПИДом, и опубликовали свои выводы в том же номере журнала. Наука.[146][147][148] Галло утверждал, что вирус, который его группа выделила от человека со СПИДом, поразительно похож на вирус. форма другим человеческие Т-лимфотропные вирусы (HTLV) его группа была изолирована первой. В 1987 году Галло признал, что вирус, который, как он утверждал, обнаружил в 1984 году, на самом деле был вирусом, присланным ему из Франции годом ранее.[149] Группа Галло назвала свой недавно выделенный вирус HTLV-III. Группа Монтанье выделила вирус у пациента с опухолью лимфатический узел шеи и физическая слабость, два классических симптома первичной ВИЧ-инфекции. Вопреки отчету группы Галло, Монтанье и его коллеги показали, что коровые белки этого вируса иммунологически отличаются от белков HTLV-I. Группа Монтанье назвала свой изолированный вирус вирусом, связанным с лимфаденопатией (LAV).[136] Поскольку эти два вируса оказались одинаковыми, в 1986 году LAV и HTLV-III были переименованы в ВИЧ.[150]
Другой группой, работавшей одновременно с группами Монтанье и Галло, была группа доктора Джея Леви. Калифорнийский университет в Сан-Франциско. Он независимо открыл вирус СПИДа в 1983 году и назвал его СПИД-ассоциированным ретровирусом (АРВ).[151] Этот вирус сильно отличался от вируса, о котором сообщили группы Монтанье и Галло. Штаммы АРВ-препаратов впервые показали гетерогенность изолятов ВИЧ, и некоторые из них остаются классическими примерами вируса СПИДа, обнаруженного в Соединенных Штатах.[152]
Происхождение
Считается, что и ВИЧ-1, и ВИЧ-2 произошли от нечеловеческих приматы в Западной и Центральной Африке, и считается, что они были переданы людям (процесс, известный как зооноз ) в начале 20 века.[153][154]
ВИЧ-1, по-видимому, возник в южной Камерун благодаря эволюции SIVcpz, вирус обезьяньего иммунодефицита (SIV), который поражает диких шимпанзе (ВИЧ-1 происходит от эндемика SIVcpz у подвида шимпанзе Пан троглодиты троглодиты ).[155][156] Ближайшим родственником ВИЧ-2 является SIVsmm, вирус закопченный мангабей (Cercocebus atys atys), Обезьяна Старого Света живущие в прибрежной зоне Западной Африки (с юга Сенегал на запад Берег Слоновой Кости ).[21] Обезьяны Нового Света такой как сова обезьяна устойчивы к инфекции ВИЧ-1, возможно, из-за геномное слияние двух генов вирусной устойчивости.[157]
Считается, что ВИЧ-1 преодолевал видовой барьер по крайней мере в трех отдельных случаях, давая начало трем группам вируса: M, N и O.[158]

Есть свидетельства того, что люди, участвующие в мясо диких животных деятельность, будь то охотники или продавцы мяса диких животных, обычно приобретает SIV.[159] Однако SIV - слабый вирус, и иммунная система человека обычно подавляет его в течение нескольких недель после заражения. Считается, что необходимо несколько последовательных передач вируса от человека к человеку, чтобы дать ему достаточно времени для мутации в ВИЧ.[160] Кроме того, из-за относительно низкой скорости передачи вируса от человека к человеку он может распространяться среди населения только при наличии одного или нескольких каналов передачи с высоким риском, которые, как считается, отсутствовали в Африке до 20 века.
Конкретные предлагаемые каналы передачи с высоким риском, позволяющие вирусу адаптироваться к людям и распространяться в обществе, зависят от предполагаемого времени перехода от животного к человеку. Генетические исследования вируса показывают, что самый недавний общий предок группы M ВИЧ-1 датируется примерно 1910 годом.[161] Сторонники этой датировки связывают эпидемию ВИЧ с появлением колониализм и рост крупных колониальных африканских городов, приводящий к социальным изменениям, включая различные модели половых контактов (особенно множественные, одновременные партнерства), распространение проституция, и сопутствующая высокая частота генитальная язва болезни (такие как сифилис ) в зарождающихся колониальных городах.[162] Хотя показатели передачи ВИЧ во время вагинального полового акта обычно невысоки, они многократно возрастают, если один из партнеров страдает от инфекция, передающаяся половым путем приводящие к генитальным язвам. Колониальные города начала 1900-х годов отличались высокой распространенностью проституции и генитальных язв до такой степени, что по состоянию на 1928 год до 45% жителей восточных районов Леопольдвиль считались проститутками, и по состоянию на 1933 год около 15% всех жителей того же города были инфицированы одной из форм сифилис.[162]
Самый ранний, хорошо задокументированный случай ВИЧ-инфекции у человека относится к 1959 г. Бельгийское Конго.[163] Вирус мог присутствовать в Соединенных Штатах еще в середине-конце 1950-х годов, когда шестнадцатилетний мужчина проявил симптомы в 1966 году и умер в 1969 году.[164]
Альтернативная точка зрения - не подкрепленная доказательствами - утверждает, что небезопасная медицинская практика в Африке в годы после Второй мировой войны, такая как нестерильное повторное использование одноразовых шприцев во время массовых кампаний вакцинации, антибиотиков и лечения малярии, была первоначальным вектором, позволившим вирус адаптироваться к людям и распространяться.[160][165][166]
Смотрите также
- Противовирусный препарат
- Открытие и разработка ингибиторов протеазы ВИЧ
- Отрицание ВИЧ / СПИДа
- Всемирный день борьбы со СПИДом
Рекомендации
- ^ Вайс Р.А. (май 1993 г.). «Как ВИЧ вызывает СПИД?». Наука. 260 (5112): 1273–9. Bibcode:1993Sci ... 260.1273W. Дои:10.1126 / science.8493571. PMID 8493571.
- ^ Douek DC, Roederer M, Koup RA (2009). «Новые концепции иммунопатогенеза СПИДа». Ежегодный обзор медицины. 60: 471–84. Дои:10.1146 / annurev.med.60.041807.123549. ЧВК 2716400. PMID 18947296.
- ^ а б Пауэлл М.К., Бенкова К., Селинджер П., Догоши М., Кинкорова Лунячкова I, Коутникова Х., Лаштикова Й., Рубичкова А., Шпуркова З., Лаклова Л., Эйс В., Шах Й., Хенеберг П. (2016). «Оппортунистические инфекции у ВИЧ-инфицированных пациентов сильно различаются по частотам и спектрам между пациентами с низким содержанием CD4 + клеток, обследованными после смерти, и пациентами с компенсацией, обследованными до смерти, независимо от эры ВААРТ». PLOS ONE. 11 (9): e0162704. Bibcode:2016PLoSO..1162704P. Дои:10.1371 / journal.pone.0162704. ЧВК 5017746. PMID 27611681.
- ^ ЮНЭЙДС, ВОЗ (Декабрь 2007 г.). «Обновленная информация об эпидемии СПИДа 2007 г.» (PDF). п. 10. Архивировано из оригинал (PDF) 22 ноября 2008 г.. Получено 12 марта, 2008.
- ^ а б c d Роджер, Элисон Дж .; Камбиано, Валентина; Бруун, Тина; Вернацца, Пьетро; Коллинз, Саймон; Деген, Олаф; и другие. (2019). «Риск передачи ВИЧ через половые отношения без презерватива в серодифференцированных гомосексуальных парах с ВИЧ-положительным партнером, принимающим супрессивную антиретровирусную терапию (ПАРТНЕР): окончательные результаты многоцентрового проспективного обсервационного исследования». Ланцет. 393 (10189): 2428–2438. Дои:10.1016 / S0140-6736 (19) 30418-0. ЧВК 6584382. PMID 31056293.
- ^ а б Эйзингер, Роберт В .; Dieffenbach, Carl W .; Фаучи, Энтони С. (2019). «Вирусная нагрузка ВИЧ и трансмиссивность ВИЧ-инфекции: неопределяемое равно непередаваемое». JAMA. 321 (5): 451–452. Дои:10.1001 / jama.2018.21167. PMID 30629090.
- ^ Мабука Дж., Ндуати Р., Одем-Дэвис К., Петерсон Д., Овербо Дж. (2012). Desrosiers RC (ред.). «ВИЧ-специфические антитела, способные вызывать ADCC, распространены в грудном молоке и связаны со сниженным риском передачи инфекции у женщин с высокой вирусной нагрузкой». Патогены PLOS. 8 (6): e1002739. Дои:10.1371 / journal.ppat.1002739. ЧВК 3375288. PMID 22719248.
- ^ Hahn, Robert A .; Инхорн, Марсия Клэр, ред. (2009). Антропология и общественное здоровье: преодоление различий в культуре и обществе (2-е изд.). Оксфорд: Издательство Оксфордского университета. п. 449. ISBN 978-0-19-537464-3. OCLC 192042314.
- ^ Мид М.Н. (2008). «Загрязняющие вещества в грудном молоке: сравнение рисков и преимуществ грудного вскармливания». Перспективы гигиены окружающей среды. 116 (10): A426–34. Дои:10.1289 / ehp.116-a426. ЧВК 2569122. PMID 18941560. Архивировано из оригинал 6 ноября 2008 г.
- ^ «Профилактика передачи ВИЧ от матери ребенку». HIV.gov. 15 мая 2017 г.. Получено 8 декабря, 2017.
 Эта статья включает текст из этого источника, который находится в всеобщее достояние.
Эта статья включает текст из этого источника, который находится в всеобщее достояние. - ^ Каннингем А.Л., Донахи Х., Харман А.Н., Ким М., Турвилл С.Г. (2010). «Манипулирование вирусами функцией дендритных клеток». Текущее мнение в микробиологии. 13 (4): 524–529. Дои:10.1016 / j.mib.2010.06.002. PMID 20598938.
- ^ Дойш, Гилад; Галлоуэй, Николь Л. К .; Гэн, Синь; Ян, Чжиюань; Монро, Кэтрин М .; Зепеда, Орландо; Хант, Питер В .; Хатано, Хирою; Совински, Стефани; Муньос-Ариас, Иса; Грин, Уорнер С. (2014). «Гибель клеток в результате пироптоза приводит к истощению Т-лимфоцитов CD4 при инфекции ВИЧ-1». Природа. 505 (7484): 509–514. Bibcode:2014Натура.505..509D. Дои:10.1038 / природа12940. ЧВК 4047036. PMID 24356306.
- ^ Гарг Х., Мохл Дж., Джоши А. (9 ноября 2012 г.). «ВИЧ-1-индуцированный апоптоз свидетеля». Вирусы. 4 (11): 3020–43. Дои:10.3390 / v4113020. ЧВК 3509682. PMID 23202514.
- ^ Кумар, Винай (2012). Базовая патология Роббинса (9-е изд.). п. 147. ISBN 978-1-4557-3787-1.
- ^ Международный комитет по таксономии вирусов (2002). «61.0.6. Лентивирус». Национальные институты здоровья. Получено 28 февраля, 2006.
- ^ Международный комитет по таксономии вирусов (2002). «61. Retroviridae». Национальные институты здоровья. Получено 28 февраля, 2006.
- ^ Леви Дж. А. (1993). «Патогенез ВИЧ и долгосрочное выживание». СПИД. 7 (11): 1401–10. Дои:10.1097/00002030-199311000-00001. PMID 8280406.
- ^ Смит Дж. А., Дэниел Р. (2006). «По пути вируса: использование ретровирусами механизмов репарации ДНК хозяина». ACS Химическая биология. 1 (4): 217–26. Дои:10.1021 / cb600131q. PMID 17163676.
- ^ а б Siliciano, R.F .; Грин, В. К. (2011). «Латентность ВИЧ». Перспективы Колд-Спринг-Харбор в медицине. 1 (1): a007096. Дои:10.1101 / cshperspect.a007096. ЧВК 3234450. PMID 22229121.
- ^ Гилберт П.Б., МакКиг И.В., Эйзен Дж., Маллинз С., Гуйе-Н.Диай А., Мбуп С., Канки П.Дж. (28 февраля 2003 г.). «Сравнение инфекционности ВИЧ-1 и ВИЧ-2 из проспективного когортного исследования в Сенегале». Статистика в медицине. 22 (4): 573–593. Дои:10.1002 / sim.1342. PMID 12590415.
- ^ а б Ривз Дж. Д., Домс Р. В. (2002). «Вирус иммунодефицита человека типа 2». Журнал общей вирусологии. 83 (Pt 6): 1253–65. Дои:10.1099/0022-1317-83-6-1253. PMID 12029140.
- ^ Макговерн С.Л., Казелли Э., Григорьев Н., Шойчет Б.К. (2002). «Общий механизм, лежащий в основе беспорядочных связей с ингибиторами виртуального и высокопроизводительного скрининга». Журнал медицинской химии. 45 (8): 1712–22. Дои:10.1021 / jm010533y. HDL:11380/977912. PMID 11931626.
- ^ По сравнению с обзором в: Фишер, Брюс; Харви, Ричард П .; Чампе, Памела С. (2007). Иллюстрированные обзоры Липпинкотта: микробиология. Иллюстрированные обзоры Липпинкотта. Хагерстаун, Мэриленд: Липпинкотт Уильямс и Уилкинс. п. 3. ISBN 978-0-7817-8215-9.
- ^ а б c d е ж грамм Разное (2008). Сборник последовательностей ВИЧ, 2008 г. Введение (PDF). Получено 31 марта, 2009.
- ^ а б c Чан, округ Колумбия, Фасс Д., Бергер Дж. М., Ким П. С. (1997). «Основная структура gp41 из гликопротеина оболочки ВИЧ» (PDF). Клетка. 89 (2): 263–73. Дои:10.1016 / S0092-8674 (00) 80205-6. PMID 9108481. S2CID 4518241.
- ^ Klein, Joshua S .; Bjorkman, Pamela J .; Ралл, Гленн Ф. (27 мая 2010 г.). «Немного и далеко: как ВИЧ может избежать авидности антител». Патогены PLOS. 6 (5): e1000908. Дои:10.1371 / journal.ppat.1000908. ЧВК 2877745. PMID 20523901.
- ^ Национальный институт здоровья (17 июня 1998 г.). «Кристаллическая структура ключевого белка ВИЧ открывает новые возможности для профилактики и лечения» (Пресс-релиз). Архивировано из оригинал 19 февраля 2006 г.. Получено 14 сентября, 2006.
- ^ Беренс, Анна-Янина; Васильевич, Снежана; Причард, Лаура К.; Харви, Дэвид Дж; Андев, Раджиндер С; Крумм, Стефани А; Струве, Уэстон Б; Купо, Альберт; Кумар, Абхинав; Зицманн, Николь; Сибрайт, Джемма Э; Крамер, Хольгер Б; Спенсер, Дэниел И.Р .; Ройл, Луиза; Ли, Чон Хён; Klasse, Per J; Бертон, Деннис Р.; Уилсон, Ян А; Уорд, Эндрю Б; Сандерс, Роджер В; Мур, Джон П.; Дур, Кэти Дж; Криспин, Макс (2016). «Состав и антигенные эффекты отдельных гликановых участков тримерного гликопротеина оболочки ВИЧ-1». Отчеты по ячейкам. 14 (11): 2695–706. Дои:10.1016 / j.celrep.2016.02.058. ЧВК 4805854. PMID 26972002.
- ^ Причард, Лаура К.; Спенсер, Дэниел И.Р .; Ройл, Луиза; Бономелли, Камилла; Сибрайт, Джемма Э; Беренс, Анна-Янина; Кулп, Дэниел В; Менис, Сергей; Крумм, Стефани А; Данлоп, Д. Кэмерон; Криспин, Дэниел Дж; Боуден, Томас А; Сканлан, Кристофер Н; Уорд, Эндрю Б; Schief, William R; Дур, Кэти Дж; Криспин, Макс (2015). «Кластеризация гликанов стабилизирует маннозный участок ВИЧ-1 и сохраняет уязвимость для широко нейтрализующих антител». Nature Communications. 6: 7479. Bibcode:2015НатКо ... 6.7479P. Дои:10.1038 / ncomms8479. ЧВК 4500839. PMID 26105115.
- ^ Причард, Лаура К.; Харви, Дэвид Дж; Бономелли, Камилла; Криспин, Макс; Дур, Кэти Дж (2015). «Клеточное и белковое гликозилирование нативной расщепленной оболочки ВИЧ-1». Журнал вирусологии. 89 (17): 8932–44. Дои:10.1128 / JVI.01190-15. ЧВК 4524065. PMID 26085151.
- ^ Криспин, Макс; Дур, Кэти Дж. (2015). «Нацеливание на гликаны, полученные из хозяина, на вирусы с оболочкой для разработки вакцины на основе антител». Текущее мнение в вирусологии. 11: 63–9. Дои:10.1016 / j.coviro.2015.02.002. ЧВК 4827424. PMID 25747313.
- ^ Жюльен, Жан-Филипп; Купо, Альберт; Сок, Девин; Stanfield, Robyn L .; Люмкис, Дмитрий; Deller, Marc C .; Классе, Пер-Йохан; Бертон, Деннис Р .; Сандерс, Роджер В. (20 декабря 2013 г.). «Кристаллическая структура растворимого расщепленного тримера оболочки ВИЧ-1». Наука. 342 (6165): 1477–1483. Bibcode:2013Научный ... 342.1477J. Дои:10.1126 / science.1245625. ISSN 1095-9203. ЧВК 3886632. PMID 24179159.
- ^ Люмкис, Дмитрий; Жюльен, Жан-Филипп; де Валь, Наталья; Купо, Альберт; Поттер, Клинтон С .; Классе, Пер-Йохан; Бертон, Деннис Р .; Сандерс, Роджер В .; Мур, Джон П. (20 декабря 2013 г.). «Крио-ЭМ структура полностью гликозилированного растворимого расщепленного тримера оболочки ВИЧ-1». Наука. 342 (6165): 1484–1490. Bibcode:2013Научный ... 342.1484L. Дои:10.1126 / science.1245627. ISSN 1095-9203. ЧВК 3954647. PMID 24179160.
- ^ Сандерс, Роджер В .; Деркинг, Рональд; Купо, Альберт; Жюльен, Жан-Филипп; Ясмин, Анила; де Валь, Наталья; Ким, Хелен Дж .; Блаттнер, Клаудиа; де ла Пенья, Альба Торрентс (1 сентября 2013 г.). «Расщепленный растворимый тример Env ВИЧ-1 нового поколения, BG505 SOSIP.664 gp140, экспрессирует несколько эпитопов для широко нейтрализующих, но не ненейтрализующих антител». Патогены PLOS. 9 (9): e1003618. Дои:10.1371 / journal.ppat.1003618. ISSN 1553-7374. ЧВК 3777863. PMID 24068931.
- ^ Причард, Лаура К .; Васильевич, Снежана; Озоровский, Габриэль; Сибрайт, Джемма Э .; Купо, Альберт; Ринге, Раджеш; Ким, Хелен Дж .; Сандерс, Роджер В .; Дур, Кэти Дж. (16 июня 2015 г.). «Структурные ограничения определяют гликозилирование тримеров оболочки ВИЧ-1». Отчеты по ячейкам. 11 (10): 1604–1613. Дои:10.1016 / j.celrep.2015.05.017. ISSN 2211-1247. ЧВК 4555872. PMID 26051934.
- ^ де Тэе, Стивен В .; Озоровский, Габриэль; Торрентс-де-ла-Пенья, Альба; Гуттман, Миклош; Жюльен, Жан-Филипп; ван ден Керкхоф, Том Л. Г. М .; Burger, Judith A .; Причард, Лаура К .; Пугач, Павел (17 декабря 2015 г.). «Иммуногенность стабилизированных тримеров оболочки ВИЧ-1 с пониженным воздействием ненейтрализующих эпитопов». Клетка. 163 (7): 1702–1715. Дои:10.1016 / j.cell.2015.11.056. ISSN 1097-4172. ЧВК 4732737. PMID 26687358.
- ^ Уэлле Д.Л., Планте I, Ландри П., Барат С., Джанель М.Э., Фламанд Л., Тремблей М.Дж., Провост П. (апрель 2008 г.). «Идентификация функциональных микроРНК, высвобождаемых посредством асимметричного процессинга TAR-элемента ВИЧ-1». Исследования нуклеиновых кислот. 36 (7): 2353–65. Дои:10.1093 / nar / gkn076. ЧВК 2367715. PMID 18299284.
- ^ Клас З, Виноград Р., Дэвис Дж., Карпио Л., Хилдрет Р., Гейдариан М., Фу С., Маккаффри Т., Мейри Э, Аяш-Рашковский М., Гилад С., Бентвич З, Кашанчи Ф (2009). «МИРНК TAR ВИЧ-1 защищает от апоптоза, изменяя экспрессию клеточных генов». Ретровирология. 6 (1): 18. Дои:10.1186/1742-4690-6-18. ЧВК 2654423. PMID 19220914.
- ^ Васудеван А.А., Смитс С.Х., Хеппнер А., Хойссингер Д., Кениг Б.В., Мюнк С. (ноябрь 2013 г.). «Структурные особенности противовирусных ДНК цитидин дезаминаз». Биологическая химия (Представлена рукопись). 394 (11): 1357–70. Дои:10.1515 / hsz-2013-0165. PMID 23787464. S2CID 4151961.
- ^ Гарсия СП, Миллер А.Д. (апрель 1991 г.). "Серин-независимая от фосфорилирования подавление CD4 клеточной поверхности с помощью nef". Природа. 350 (6318): 508–11. Bibcode:1991Натура.350..508Г. Дои:10.1038 / 350508a0. PMID 2014052. S2CID 1628392.
- ^ Schwartz O, Maréchal V, Le Gall S, Lemonnier F, Heard JM (март 1996 г.). «Эндоцитоз молекул класса I главного комплекса гистосовместимости индуцируется белком Nef ВИЧ-1». Природа Медицина. 2 (3): 338–42. Дои:10,1038 / нм0396-338. PMID 8612235. S2CID 7461342.
- ^ Stumptner-Cuvelette P, Morchoisne S, Dugast M, Le Gall S, Raposo G, Schwartz O, Benaroch P (октябрь 2001 г.). «Nef ВИЧ-1 ухудшает презентацию антигена MHC класса II и поверхностную экспрессию». Труды Национальной академии наук Соединенных Штатов Америки. 98 (21): 12144–9. Bibcode:2001ПНАС ... 9812144С. Дои:10.1073 / pnas.221256498. ЧВК 59782. PMID 11593029.
- ^ Аррильдт, Кэтрин Твигг; Джозеф, Сара Бет; Swanstrom, Рональд (март 2012). «Белок Env ВИЧ-1: разноцветный покров». Текущие отчеты о ВИЧ / СПИДе. 9 (Текущие отчеты о ВИЧ / СПИДе): 53–63. Дои:10.1007 / s11904-011-0107-3. ЧВК 3658113. PMID 22237899.
- ^ а б Berger EA, Doms RW, Fenyö EM, Korber BT, Littman DR, Moore JP, Sattentau QJ, Schuitemaker H, Sodroski J, Weiss RA (1998). «Новая классификация ВИЧ-1». Природа. 391 (6664): 240. Bibcode:1998Натура.391..240Б. Дои:10.1038/34571. PMID 9440686. S2CID 2159146.
- ^ а б c Коакли Э., Петропулос С. Дж., Уиткомб Дж. М. (2005). «Оценка использования корецептора ch vbgemokine при ВИЧ». Современное мнение об инфекционных заболеваниях. 18 (1): 9–15. Дои:10.1097/00001432-200502000-00003. PMID 15647694. S2CID 30923492.
- ^ Денг Х., Лю Р., Эллмайер В., Чхве С., Унутмаз Д., Буркхарт М., Ди Марцио П., Мармон С., Саттон Р. Э., Хилл К. М., Дэвис С. Б., Пейпер С. К., Шалл Т. Дж., Литтман Д. Р., Ландау Н. Р. (1996). «Идентификация основного корецептора для первичных изолятов ВИЧ-1». Природа. 381 (6584): 661–6. Bibcode:1996Натура.381..661D. Дои:10.1038 / 381661a0. PMID 8649511. S2CID 37973935.
- ^ Фен Й, Бродер CC, Кеннеди PE, Бергер EA (1996). «Входной кофактор ВИЧ-1: функциональное клонирование кДНК семимембранного рецептора, сопряженного с G-белком». Наука. 272 (5263): 872–7. Bibcode:1996Наука ... 272..872F. Дои:10.1126 / science.272.5263.872. PMID 8629022. S2CID 44455027.
- ^ Knight SC, Macatonia SE, Patterson S (1990). «ВИЧ-инфекция дендритных клеток». Международный обзор иммунологии. 6 (2–3): 163–75. Дои:10.3109/08830189009056627. PMID 2152500.
- ^ Тан Дж, Каслоу Р.А. (2003). «Влияние генетики хозяина на ВИЧ-инфекцию и прогрессирование заболевания в эпоху высокоактивной антиретровирусной терапии». СПИД. 17 (Приложение 4): S51 – S60. Дои:10.1097/00002030-200317004-00006. PMID 15080180.
- ^ Чжу Т., Мо Х, Ван Н., Нам Д.С., Цао И, Куп Р.А., Хо Д.Д. (1993). «Генотипическая и фенотипическая характеристика больных ВИЧ-1 с первичной инфекцией». Наука. 261 (5125): 1179–81. Bibcode:1993Научный ... 261.1179Z. Дои:10.1126 / science.8356453. PMID 8356453.
- ^ van't Wout AB, Kootstra NA, Mulder-Kampinga GA, Albrecht-van Lent N, Scherpbier HJ, Veenstra J, Boer K, Coutinho RA, Miedema F, Schuitemaker H (1994). «Макрофаготропные варианты инициируют инфицирование вирусом иммунодефицита человека типа 1 после половой, парентеральной и вертикальной передачи». Журнал клинических исследований. 94 (5): 2060–7. Дои:10.1172 / JCI117560. ЧВК 294642. PMID 7962552.
- ^ Чжу Т., Ван Н., Карр А., Нам Д.С., Мур-Янковски Р., Купер Д.А., Хо Д.Д. (1996). «Генетическая характеристика вируса иммунодефицита человека 1 типа в крови и генитальных выделениях: доказательства компартментализации и отбора вирусов при передаче половым путем». Журнал вирусологии. 70 (5): 3098–107. Дои:10.1128 / JVI.70.5.3098-3107.1996. ЧВК 190172. PMID 8627789.
- ^ Клестер П., Малжкович И., Каспер С., Карленор Э., Линдгрен С., Навер Л., Болин А.Б., Фенё Е.М., Лейтнер Т., Эрнст А. (2005). «Фенотип X4 ВИЧ-типа 1 происходит от R5 у двух детей матерей, носящих X4, и не связан с передачей». Исследования СПИДа и ретровирусы человека. 21 (5): 371–8. Дои:10.1089 / aid.2005.21.371. PMID 15929699.
- ^ Мур Дж. П. (1997). «Корецепторы: значение для патогенеза и терапии ВИЧ». Наука. 276 (5309): 51–2. Дои:10.1126 / science.276.5309.51. PMID 9122710. S2CID 33262844.
- ^ Карлссон А., Парсмир К., Аперия К., Сандстрём Э, Феньё Э.М., Альберт Дж. (1994). «Тропизм клеток МТ-2 изолятов вируса иммунодефицита человека типа 1 как маркер ответа на лечение и развития лекарственной устойчивости». Журнал инфекционных болезней. 170 (6): 1367–75. Дои:10.1093 / infdis / 170.6.1367. PMID 7995974.
- ^ Koot M, van 't Wout AB, Kootstra NA, de Goede RE, Tersmette M, Schuitemaker H (1996). «Связь между изменениями в клеточной нагрузке, эволюцией вирусного фенотипа и клональным составом вирусных популяций в ходе инфицирования вирусом иммунодефицита человека 1 типа». Журнал инфекционных болезней. 173 (2): 349–54. Дои:10.1093 / infdis / 173.2.349. PMID 8568295.
- ^ Чейни К., Макнайт А. (2010). «Тропизм и болезнь ВИЧ-2». Лентивирусы и макрофаги: молекулярные и клеточные взаимодействия. Caister Academic Press. ISBN 978-1-904455-60-8.[страница нужна ]
- ^ а б c d е ж грамм Чан, округ Колумбия, Ким PS (1998). «Поступление ВИЧ и его подавление». Клетка. 93 (5): 681–4. Дои:10.1016 / S0092-8674 (00) 81430-0. PMID 9630213. S2CID 10544941.
- ^ а б c d е ж Вятт Р., Содроски Дж. (1998). «Гликопротеины оболочки ВИЧ-1: фузогены, антигены и иммуногены». Наука. 280 (5371): 1884–8. Bibcode:1998Sci ... 280.1884W. Дои:10.1126 / science.280.5371.1884. PMID 9632381.
- ^ а б Артос Дж., Чикала С., Мартинелли Э, Маклеод К., Ван Рик Д., Вей Д., Сяо З., Винстра Т. Д., Конрад Т. П., Лемпицки Р. А., Маклафлин С., Паскуччио М., Гопаул Р., МакНалли Дж., Круз С. К., Ченсоплано Н., Чанг E, Reitano KN, Kottilil S, Goode DJ, Fauci AS (2008). «Белок оболочки ВИЧ-1 связывается и передает сигналы через интегрин альфа (4) бета (7), рецептор самонаведения слизистой оболочки кишечника для периферических Т-клеток». Иммунология природы. 9 (3): 301–9. Дои:10.1038 / ni1566. PMID 18264102. S2CID 205361178.
- ^ а б Папа М, Хаазе А.Т. (2003). «Передача, острая инфекция ВИЧ-1 и поиск стратегий предотвращения инфекции». Природа Медицина. 9 (7): 847–52. Дои:10,1038 / нм0703-847. PMID 12835704. S2CID 26570505.
- ^ Хедике Дж., Браун С., Нагави М. Х. (август 2009 г.). «Специфический для мозга фактор FEZ1 является определяющим фактором восприимчивости нейронов к инфекции ВИЧ-1». Труды Национальной академии наук. 106 (33): 14040–14045. Bibcode:2009PNAS..10614040H. Дои:10.1073 / pnas.0900502106. ЧВК 2729016. PMID 19667186.
- ^ Дэке Дж, Факлер О.Т., Диттмар М.Т., Кройсслих Г.Г. (2005). «Участие клатрин-опосредованного эндоцитоза в проникновении вируса иммунодефицита человека типа 1». Журнал вирусологии. 79 (3): 1581–1594. Дои:10.1128 / jvi.79.3.1581-1594.2005. ЧВК 544101. PMID 15650184.
- ^ Мияучи К., Ким Й., Латинович О., Морозов В., Меликян ГБ (2009). «ВИЧ проникает в клетки посредством эндоцитоза и динамин-зависимого слияния с эндосомами». Клетка. 137 (3): 433–444. Дои:10.1016 / j.cell.2009.02.046. ЧВК 2696170. PMID 19410541.
- ^ Кох П., Лампе М., Годинез В.Дж., Мюллер Б., Рор К., Кройсслих Г.Г., Леманн М.Дж. (2009). «Визуализация слияния псевдотипированных частиц ВИЧ-1 в реальном времени с помощью микроскопии живых клеток». Ретровирология. 6: 84. Дои:10.1186/1742-4690-6-84. ЧВК 2762461. PMID 19765276.
- ^ Торли Дж. А., Маккитинг Дж. А., Раппопорт Дж. З. (2010). "Механизм проникновения вирусов: крадется в парадную дверь". Протоплазма. 244 (1–4): 15–24. Дои:10.1007 / s00709-010-0152-6. ЧВК 3038234. PMID 20446005.
- ^ Перманьер М, Баллана Э, Эсте Ж.А. (2010). «Эндоцитоз ВИЧ: все идет». Тенденции в микробиологии. 18 (12): 543–551. Дои:10.1016 / j.tim.2010.09.003. PMID 20965729.
- ^ а б c Чжэн Ю.Х., Ловсин Н., Петерлин Б.М. (2005). «Недавно идентифицированные факторы хозяина модулируют репликацию ВИЧ». Письма иммунологии. 97 (2): 225–34. Дои:10.1016 / j.imlet.2004.11.026. PMID 15752562.
- ^ «IV. Вирусы> F. Жизненные циклы вирусов животных> 3. Жизненный цикл ВИЧ». Домашняя страница микробиологии Дока Кайзера. Общественный колледж округа Балтимор. Январь 2008. Архивировано с оригинал 26 июля 2010 г.
- ^ Хискотт Дж., Квон Х., Женин П. (2001). «Враждебные поглощения: вирусное присвоение пути NF-kB». Журнал клинических исследований. 107 (2): 143–151. Дои:10.1172 / JCI11918. ЧВК 199181. PMID 11160127.
- ^ Поллард В.В., Малим М.Х. (1998). «Белок HIV-1 Rev». Ежегодный обзор микробиологии. 52: 491–532. Дои:10.1146 / annurev.micro.52.1.491. PMID 9891806.
- ^ Butsch, M .; Борис-Лори, К. (2002). «Судьба несплицированной ретровирусной РНК: рибосома и / или вирион?». Журнал вирусологии. 76 (7): 3089–94. Дои:10.1128 / JVI.76.7.3089-3094.2002. ЧВК 136024. PMID 11884533.
- ^ Хельмунд, Крис; Левер, Эндрю М. Л. (14 июля 2016 г.). «Координация упаковки геномной РНК с вирусной сборкой в ВИЧ-1». Вирусы. 8 (7): 192. Дои:10.3390 / v8070192. ISSN 1999-4915. ЧВК 4974527. PMID 27428992.
- ^ Soto-Rifo, R .; Лимузен, Т .; Rubilar, P. S .; Ricci, E. P .; Décimo, D .; Moncorgé, O .; Trabaud, M. A .; André, P .; Cimarelli, A .; Ольманн, Т. (2011). «Различные эффекты структуры TAR на трансляцию геномных РНК ВИЧ-1 и ВИЧ-2». Исследования нуклеиновых кислот. 40 (6): 2653–2667. Дои:10.1093 / нар / gkr1093. ЧВК 3315320. PMID 22121214.
- ^ Saad, Jamil S .; Мурио, Дельфин М. (28 июля 2015 г.). Роль липидов в сборке вирусов. Frontiers Media SA. ISBN 9782889195824.
- ^ Ricci, E. P .; Herbreteau, C.H .; Decimo, D .; Schaupp, A .; Датта, С. А. К .; Rein, A .; Darlix, J. -L .; Ольманн, Т. (2008). «Экспрессия геномной РНК ВИЧ-2 in vitro контролируется тремя отдельными внутренними входными сегментами рибосомы, которые регулируются протеазой ВИЧ и полипротеином Gag». РНК. 14 (7): 1443–55. Дои:10.1261 / rna.813608. ЧВК 2441975. PMID 18495939.
- ^ а б Ху WS, Темин Х.М. (1990). «Ретровирусная рекомбинация и обратная транскрипция». Наука. 250 (4985): 1227–33. Bibcode:1990Sci ... 250.1227H. Дои:10.1126 / science.1700865. PMID 1700865.
- ^ а б Шарпантье С., Нора Т., Тенайон О, Клавель Ф, Ханс А.Дж. (2006). «Обширная рекомбинация квазивидов вируса иммунодефицита человека типа 1 вносит важный вклад в вирусное разнообразие у отдельных пациентов». Журнал вирусологии. 80 (5): 2472–82. Дои:10.1128 / JVI.80.5.2472-2482.2006. ЧВК 1395372. PMID 16474154.
- ^ Нора Т., Шарпантье С., Тенайлон О, Ходе С., Клавель Ф, Ханс А.Дж. (2007). «Вклад рекомбинации в эволюцию вирусов иммунодефицита человека, выражающих устойчивость к антиретровирусной терапии». Журнал вирусологии. 81 (14): 7620–8. Дои:10.1128 / JVI.00083-07. ЧВК 1933369. PMID 17494080.
- ^ Чен Дж, Пауэлл Д., Ху В.С. (2006). «Высокая частота генетической рекомбинации - общая черта репликации лентивирусов приматов». Журнал вирусологии. 80 (19): 9651–8. Дои:10.1128 / JVI.00936-06. ЧВК 1617242. PMID 16973569.
- ^ а б Bonhoeffer S, Chappey C, Parkin NT, Whitcomb JM, Petropoulos CJ (2004). «Доказательства положительного эпистаза при ВИЧ-1». Наука. 306 (5701): 1547–50. Bibcode:2004Наука ... 306.1547B. Дои:10.1126 / science.1101786. PMID 15567861. S2CID 45784964.
- ^ Israël N, Gougerot-Pocidalo MA (1997). «Окислительный стресс при инфекции вируса иммунодефицита человека». Клеточные и молекулярные науки о жизни. 53 (11–12): 864–70. Дои:10.1007 / с000180050106. PMID 9447238. S2CID 22663454.
- ^ Мичод Р.Э., Бернштейн Х., Недельку А.М. (май 2008 г.). «Адаптивное значение секса у микробных возбудителей» (PDF). Инфекция, генетика и эволюция. 8 (3): 267–85. Дои:10.1016 / j.meegid.2008.01.002. PMID 18295550.
- ^ Hallenberger S, Bosch V, Angliker H, Shaw E, Klenk HD, Garten W. (26 ноября 1992 г.). «Ингибирование опосредованной фурином активации расщепления гликопротеина gp160 ВИЧ-1». Природа. 360 (6402): 358–61. Bibcode:1992Натура. 360..358H. Дои:10.1038 / 360358a0. PMID 1360148. S2CID 4306605.
- ^ Гельдерблом HR (1997). «Тонкая структура ВИЧ и ВИО» (PDF). В Лос-Аламосской национальной лаборатории (ред.). Сборник последовательностей ВИЧ. Лос-Аламосская национальная лаборатория. С. 31–44.
- ^ а б c d Чжан С., Чжоу С., Гроппелли Э, Пеллегрино П., Уильямс И., Броу П., Цепь Б.М., Веселая С. (2015). «Гибридные механизмы распространения и активация Т-лимфоцитов определяют динамику инфицирования ВИЧ-1». PLOS вычислительная биология. 11 (4): e1004179. arXiv:1503.08992. Bibcode:2015PLSCB..11E4179Z. Дои:10.1371 / journal.pcbi.1004179. ЧВК 4383537. PMID 25837979.
- ^ а б Веселый К., Кашефи К., Холлинсхед М., Саттентау QJ (2004). «Перенос клеток ВИЧ-1 в клетки через Env-индуцированный актин-зависимый синапс». Журнал экспериментальной медицины. 199 (2): 283–293. Дои:10.1084 / jem.20030648. ЧВК 2211771. PMID 14734528.
- ^ Саттентау Q (2008). «Избегая пустоты: распространение вирусов от клетки к клетке». Обзоры природы Микробиология. 6 (11): 815–826. Дои:10.1038 / nrmicro1972. PMID 18923409. S2CID 20991705.
- ^ Дункан CJ, Рассел Р.А., Саттентау QJ (2013). «Высокая множественность передачи ВИЧ-1 от клетки к клетке от макрофагов к CD4 + Т-клеткам ограничивает антиретровирусную эффективность». СПИД. 27 (14): 2201–2206. Дои:10.1097 / QAD.0b013e3283632ec4. ЧВК 4714465. PMID 24005480.
- ^ Севальд X, Гонсалес Д.Г., Хаберман А.М., Мотес В. (2012). «Визуализация вирусологических синапсов in vivo». Nature Communications. 3: 1320. Bibcode:2012НатКо ... 3.1320S. Дои:10.1038 / ncomms2338. ЧВК 3784984. PMID 23271654.
- ^ Сигал А., Ким Дж. Т., Балаш А. Б., Декель Е., Майо А., Майло Р., Балтимор Д. (2011). «Распространение ВИЧ от клетки к клетке позволяет продолжать репликацию, несмотря на антиретровирусную терапию». Природа. 477 (7362): 95–98. Bibcode:2011Натура 477 ... 95S. Дои:10.1038 / природа10347. PMID 21849975. S2CID 4409389.
- ^ а б c d Робертсон Д.Л., Хан Б.Х., Sharp PM (1995). «Рекомбинация в вирусах СПИДа». Журнал молекулярной эволюции. 40 (3): 249–59. Bibcode:1995JMolE..40..249R. Дои:10.1007 / BF00163230. PMID 7723052. S2CID 19728830.
- ^ Рамбаут А., Посада Д., Крэндалл К.А., Холмс ЕС (январь 2004 г.). «Причины и последствия эволюции ВИЧ». Природа Обзоры Генетика. 5 (52–61): 52–61. Дои:10.1038 / nrg1246. PMID 14708016. S2CID 5790569.
- ^ Перельсон А.С., Рибейро Р.М. (октябрь 2008 г.). «Оценка эффективности препарата и вирусных динамических параметров: ВИЧ и ВГС». Статистика в медицине. 27 (23): 4647–57. Дои:10.1002 / sim.3116. PMID 17960579.
- ^ а б Содора Д.Л., Аллан Дж. С., Апетрей К., Бренчли Дж. М., Дуек, округ Колумбия, Эльсе Дж. Г., Эстес Дж. Д., Хан Б. Х., Хирш В. М., Каур А., Кирхгоф Ф., Мюллер-Трутвин М., Пандреа И., Шмитц Дж. Э., Сильвестри Г. (2009). «К вакцине против СПИДа: уроки естественного заражения вирусом обезьяньего иммунодефицита африканских приматов-хозяев». Природа Медицина. 15 (8): 861–865. Дои:10.1038 / нм.2013. ЧВК 2782707. PMID 19661993.
- ^ Holzammer S, Holznagel E, Kaul A, Kurth R, Norley S (2001). «Высокие вирусные нагрузки у африканских зеленых мартышек, инфицированных естественным и экспериментальным путем SIVagm». Вирусология. 283 (2): 324–31. Дои:10.1006 / viro.2001.0870. PMID 11336557.
- ^ Kurth, R .; Норли, С. (1996). «Почему у естественных хозяев ВИО не развивается обезьяний СПИД?». Журнал исследований NIH. 8: 33–37.
- ^ Байер М., Диттмар М.Т., Цичутек К., Курт Р. (1991). «Развитие vivo генетической изменчивости вируса иммунодефицита обезьян». Труды Национальной академии наук Соединенных Штатов Америки. 88 (18): 8126–30. Bibcode:1991PNAS ... 88.8126B. Дои:10.1073 / пнас.88.18.8126. ЧВК 52459. PMID 1896460.
- ^ Дэниел Мэриленд, Король Н.В., Летвин Н.Л., Хант Р.Д., Сегал П.К., Дерозье Р.К. (1984). «Новый ретровирус типа D, выделенный от макак с синдромом иммунодефицита». Наука. 223 (4636): 602–5. Bibcode:1984Научный ... 223..602D. Дои:10.1126 / science.6695172. PMID 6695172.
- ^ а б Кил Б.Ф., Джонс Дж.Х., Терио К.А., Эстес Дж.Д., Рудичелл Р.С., Уилсон М.Л., Ли Y, Learn GH, Beasley TM, Шумахер-Станки Дж., Вроблевски Е., Моссер А., Рафаэль Дж., Каменя С., Лонсдорф Е.В., Трэвис Д.А., Мленгея Т., Кинсел М.Дж., Эльсе Дж. Г., Сильвестри Дж., Гудолл Дж., Шарп П.М., Шоу Г.М., Пусей А.Э., Хан Б.Х. (2009). «Повышенная смертность и СПИД-подобная иммунопатология у диких шимпанзе, инфицированных SIVcpz». Природа. 460 (7254): 515–519. Bibcode:2009Натура.460..515K. Дои:10.1038 / nature08200. ЧВК 2872475. PMID 19626114.
- ^ Schindler M, Münch J, Kutsch O, Li H, Santiago ML, Bibollet-Ruche F, Müller-Trutwin MC, Novembre FJ, Peeters M, Courgnaud V, Bailes E, Roques P, Sodora DL, Silvestri G, Sharp PM, Hahn BH, Кирхгоф Ф (2006). «Опосредованное Nef подавление активации Т-клеток было потеряно в лентивирусной линии, которая дала начало ВИЧ-1». Клетка. 125 (6): 1055–67. Дои:10.1016 / j.cell.2006.04.033. PMID 16777597. S2CID 15132918.
- ^ Томсон М.М., Перес-Альварес Л., Нахера Р. (2002). «Молекулярная эпидемиология генетических форм ВИЧ-1 и ее значение для разработки вакцин и терапии». Ланцетные инфекционные болезни. 2 (8): 461–471. Дои:10.1016 / S1473-3099 (02) 00343-2. PMID 12150845.
- ^ Карр Дж. К., Фоли Б. Т., Лейтнер Т., Салминен М., Корбер Б., МакКатчан Ф (1998). «Контрольные последовательности, представляющие основное генетическое разнообразие ВИЧ-1 в пандемии» (PDF). В Лос-Аламосской национальной лаборатории (ред.). Сборник последовательностей ВИЧ. Лос-Аламос, Нью-Мексико: Лос-Аламосская национальная лаборатория. С. 10–19.
- ^ Османов С., Патту С., Уокер Н., Швардлендер Б., Эспарза Дж. (2002). «Предполагаемое глобальное распространение и региональное распространение генетических подтипов ВИЧ-1 в 2000 году». Журнал синдромов приобретенного иммунодефицита. 29 (2): 184–190. Дои:10.1097/00042560-200202010-00013. PMID 11832690. S2CID 12536801.
- ^ Перрин Л., Кайзер Л., Йерли С. (2003). «Путешествие и распространение генетических вариантов ВИЧ-1». Ланцетные инфекционные болезни. 3 (1): 22–27. Дои:10.1016 / S1473-3099 (03) 00484-5. PMID 12505029.
- ^ а б Plantier JC, Leoz M, Dickerson JE, De Oliveira F, Cordonnier F, Lemée V, Damon F, Robertson DL, Simon F (август 2009 г.). «Новый вирус иммунодефицита человека, полученный от горилл». Природа Медицина. 15 (8): 871–2. Дои:10.1038 / нм.2016. PMID 19648927. S2CID 76837833. Сложить резюме.
- ^ Кил Б.Ф., Ван Хеуверсвин Ф., Ли И, Бейлес Э, Такехиса Дж., Сантьяго М.Л., Биболлет-Руш Ф, Чен И, Уэйн Л.В., Льежуа Ф, Лоул С., Нголе Э.М., Бьенвеню Y, Делапорте Э, Брукфилд Дж. Ф., Шарп П.М. , Shaw GM, Peeters M, Hahn BH (28 июля 2006 г.). «Шимпанзе - резервуары пандемического и непандемического ВИЧ-1». Наука. 313 (5786): 523–6. Bibcode:2006Научная ... 313..523K. Дои:10.1126 / science.1126531. ЧВК 2442710. PMID 16728595.
- ^ а б c d Kumaranayake, L .; Уоттс, К. (2001). «Распределение ресурсов и установление приоритетов мероприятий по ВИЧ / СПИДу: борьба с генерализованной эпидемией в странах Африки к югу от Сахары». Журнал международного развития. 13 (4): 451–466. Дои:10.1002 / jid.797.
- ^ Клейнман С (сентябрь 2004 г.). «Информация для пациентов: сдача и переливание крови». Своевременно. Архивировано из оригинал 12 апреля 2008 г.
- ^ а б Центры по контролю и профилактике заболеваний (2001 г.). «Пересмотренное руководство по консультированию, тестированию и направлению на ВИЧ». Рекомендации и отчеты MMWR. 50 (RR – 19): 1–57. PMID 11718472.
- ^ Селум С.Л., Кумбс Р.В., Лафферти В., Инуи Т.С., Луи П.Х., Гейтс, Калифорния, МакКриди Б.Дж., Иган Р., Гроув Т., Александр С. (1991). «Неопределенный вестерн-блоттинг вируса иммунодефицита человека 1 типа: риск сероконверсии, специфичность дополнительных тестов и алгоритм оценки». Журнал инфекционных болезней. 164 (4): 656–664. Дои:10.1093 / infdis / 164.4.656. PMID 1894929.
- ^ «Сравнение стран :: ВИЧ / СПИД - смертельные случаи». The World Factbook, Центральное разведывательное управление.
- ^ Чоу, Роджер; Селф, Шелли; Дана, Трейси; Бугацос, Кристина; Захер, Бернадетт; Блазина, Ян; Кортуис, П. Тодд (20 ноября 2012 г.). «Скрининг на ВИЧ: систематический обзор для обновления рекомендаций Целевой группы США по профилактическим услугам от 2005 г.». Анналы внутренней медицины. 157 (10): 706–718. Дои:10.7326/0003-4819-157-10-201211200-00007. ISSN 1539-3704. PMID 23165662. S2CID 27494096.
- ^ Чоу Р., Хаффман Л. Х., Фу Р., Смитс А. К., Кортуис П. Т. (июль 2005 г.). «Скрининг на ВИЧ: обзор доказательств для Целевой группы США по профилактическим услугам». Анналы внутренней медицины. 143 (1): 55–73. Дои:10.7326/0003-4819-143-1-200507050-00010. PMID 15998755.
- ^ Толле М.А., Шварцвальд Х.Л. (15 июля 2010 г.). «Постконтактная профилактика вируса иммунодефицита человека». Американский семейный врач. 82 (2): 161–6. PMID 20642270.
- ^ «Краткое справочное руководство - лабораторное тестирование для диагностики ВИЧ-инфекции: обновленные рекомендации» (PDF). cdc.gov. Департамент здравоохранения штата Нью-Йорк. 27 июня 2014 г. С. 1–2. Архивировано из оригинал (PDF) 2 марта 2017 г.. Получено 13 апреля, 2017.
- ^ «Лечение ВИЧ: лекарства от ВИЧ, одобренные FDA». AIDSinfo.
- ^ Швейцарская национальная комиссия по СПИДу (15 октября 2016 г.). "Швейцарское заявление". ВИЧ i-Base. Получено 2 апреля, 2019.
- ^ Ланцет ВИЧ (ноябрь 2017 г.). «U = U взлетает в 2017 году». От редакции. Ланцет ВИЧ. 44 (11): e475. Дои:10.1016 / С2352-3018 (17) 30183-2. PMID 29096785.
- ^ "Не могу передать это дальше". Терренс Хиггинс Trust. 2019. В архиве с оригинала 7 апреля 2019 г.. Получено 2 апреля, 2019.
- ^ Бавингтон, Бенджамин Р .; Пинто, Энджи Н .; Пханупхак, Ниттая; Гринштейн, Беатрис; Prestage, Garrett P .; Заблоцкая-Манос Ирина Б .; и другие. (2018). «Подавление вируса и передача ВИЧ в серодискордантных мужских парах: международное проспективное обсервационное когортное исследование». Ланцет ВИЧ. 5 (8): e438 – e447. Дои:10.1016 / С2352-3018 (18) 30132-2. PMID 30025681.
- ^ Роджер, Элисон Дж .; Камбиано, Валентина; Бруун, Тина; Вернацца, Пьетро; Коллинз, Саймон; ван Лунзен, Ян; и другие. (2016). «Сексуальная активность без презервативов и риск передачи ВИЧ в серодифферентных парах, когда ВИЧ-положительный партнер использует подавляющую антиретровирусную терапию». JAMA. 316 (2): 171–181. Дои:10.1001 / jama.2016.5148. PMID 27404185.
- ^ Роджер, А. (для исследовательской группы PARTNER) (июль 2018 г.). Риск передачи ВИЧ при сексе без презерватива в парах МСМ с подавляющей АРТ: исследование PARTNER2 расширило результаты среди мужчин-геев. AIDS2018: 22-я Международная конференция по СПИДу. Амстердам, Нидерланды. Получено 2 апреля, 2019.
- ^ а б c Хоффман, Хиллари (10 января 2019 г.). «Наука ясна: с ВИЧ нераспознаваемый означает непередаваемый» (Пресс-релиз). Национальные институты здоровья. Национальный институт аллергии и инфекционных заболеваний. Получено 3 мая, 2019.
Директор NIAID Энтони С. Фаучи, доктор медицинских наук, и его коллеги обобщают результаты крупных клинических испытаний и когортных исследований, подтверждающих, что U = U. Знаковое клиническое исследование HPTN 052, финансируемое Национальным институтом здравоохранения, показало, что между серодифферентными к ВИЧ гетеросексуальными парами не было связанной передачи ВИЧ, когда у партнера, живущего с ВИЧ, вирусная нагрузка была длительно подавлена. Впоследствии исследования PARTNER и Opposites Attract подтвердили эти выводы и распространили их на пары мужчина-мужчина. ... Успех U = U как метода профилактики ВИЧ зависит от достижения и поддержания неопределяемой вирусной нагрузки путем ежедневного приема АРТ в соответствии с предписаниями.
- ^ Коэн, Майрон С.; Chen, Ying Q .; Макколи, Мэрибет; Гэмбл, Тереза; Hosseinipour, Mina C .; Кумарасами, Нагалингесваран; и другие. (2016). «Антиретровирусная терапия для профилактики передачи ВИЧ-1». N. Engl. J. Med. 375 (9): 830–839. Дои:10.1056 / NEJMoa1600693. ЧВК 5049503. PMID 27424812.
- ^ Ходсон, Мэтью (17 ноября 2017 г.). U = U: разговор с пациентами о риске передачи (PDF). Осенняя конференция Британской ассоциации по ВИЧ 2017 г.. Получено 3 мая, 2019. (Абстрактные для презентации от имени NAM / aidsmap )
- ^ «Консенсусное заявление: риск передачи ВИЧ половым путем от человека, живущего с ВИЧ, с неопределяемой вирусной нагрузкой». Кампания по предотвращению доступа. 21 июля 2016 г.. Получено 2 апреля, 2019. Примечание: Когда заявление и список одобрений были получены, последний раз он обновлялся 23 августа 2018 года и включал «более 850 организаций из почти 100 стран».
- ^ Бозли, Сара; Девлин, Ханна (3 мая 2019 г.). «Конец СПИДу на горизонте, поскольку огромное исследование показало, что наркотики останавливают передачу ВИЧ». Хранитель. Получено 3 мая, 2019.
- ^ Чжу, Цзя; Хладик, Флориан; Вудворд, Аманда; Клок, Алексис; Пэн, Дао; Джонстон, Кристина; Ремингтон, Майкл; Магарет, Амалия; Koelle, Дэвид М .; Уолд, Анна; Кори, Лоуренс (август 2009 г.). «Сохранение рецептор-положительных клеток ВИЧ-1 после реактивации HSV-2: потенциальный механизм увеличения приобретения ВИЧ-1». Природа Медицина. 15 (8): 886–892. Дои:10.1038 / нм.2006. ISSN 1078-8956. ЧВК 2723183. PMID 19648930.
- ^ Looker, Кэтрин Дж .; Elmes, Jocelyn A. R .; Gottlieb, Sami L .; Шиффер, Джошуа Т .; Викерман, Питер; Тернер, Кэтрин М. Э .; Бойли, Мари-Клод (декабрь 2017 г.). «Влияние инфекции HSV-2 на последующее заражение ВИЧ: обновленный систематический обзор и метаанализ». Ланцет. Инфекционные заболевания. 17 (12): 1303–1316. Дои:10.1016 / S1473-3099 (17) 30405-X. ISSN 1474-4457. ЧВК 5700807. PMID 28843576.
- ^ "В этот день". Новости и записи. 18 мая 2020 г. с. 2А.
- ^ Mandell, Gerald L .; Беннетт, Джон Э .; Долин, Рафаэль, ред. (2010). «Глава 169». Принципы и практика Манделла, Дугласа и Беннета в отношении инфекционных болезней (7-е изд.). Филадельфия: Черчилль Ливингстон / Эльзевьер. ISBN 978-0-443-06839-3.[страница нужна ]
- ^ Готтлиб М.С. (2006). "Пневмоцистная пневмония - Лос-Анджелес. 1981". Американский журнал общественного здравоохранения. 96 (6): 980–1, обсуждение 982–3. Дои:10.2105 / AJPH.96.6.980. ЧВК 1470612. PMID 16714472. В архиве из оригинала от 22 апреля 2009 г.
- ^ Фридман-Кин А.Е. (октябрь 1981 г.). «Синдром диссеминированной саркомы Капоши у молодых гомосексуалистов». Журнал Американской академии дерматологии. 5 (4): 468–71. Дои:10.1016 / S0190-9622 (81) 80010-2. PMID 7287964.
- ^ Хаймс КБ, Чунг Т., Грин Дж. Б., Проза Н. С., Маркус А., Баллард Н., Уильям Д. К., Лаубенштейн Л. Дж. (Сентябрь 1981 г.). «Саркома Капоши у гомосексуальных мужчин - сообщение о восьми случаях». Ланцет. 2 (8247): 598–600. Дои:10.1016 / S0140-6736 (81) 92740-9. PMID 6116083. S2CID 43529542.
- ^ а б Басавапатруни А., Андерсон К.С. (декабрь 2007 г.). «Обратная транскрипция пандемии ВИЧ-1». Журнал FASEB. 21 (14): 3795–3808. Дои:10.1096 / fj.07-8697rev. PMID 17639073. S2CID 24960391.
- ^ Ледерберг, Джошуа, изд. (2000). Энциклопедия микробиологии (2-е изд.). Берлингтон: Эльзевир. п. 106. ISBN 978-0-08-054848-7. Получено 9 июня, 2016.
- ^ Центры по контролю за заболеваниями (1982). «Стойкая генерализованная лимфаденопатия среди мужчин-гомосексуалистов». Еженедельный отчет о заболеваемости и смертности. 31 (19): 249–251. PMID 6808340.
- ^ Барре-Синусси Ф., Шерманн Дж. К., Рей Ф., Нугейр М. Т., Шамарэ С., Грюст Дж., Доге С., Акслер-Блин С., Везине-Брун Ф., Рузиу С., Розенбаум В., Монтанье Л. (1983). «Выделение Т-лимфотропного ретровируса от пациента с риском синдрома приобретенного иммунодефицита (СПИД)». Наука. 220 (4599): 868–871. Bibcode:1983Научный ... 220..868B. Дои:10.1126 / science.6189183. PMID 6189183. S2CID 390173.
- ^ а б Центры по контролю за заболеваниями (1982). «Оппортунистические инфекции и саркома Капоши среди гаитян в США». Еженедельный отчет о заболеваемости и смертности. 31 (26): 353–354, 360–361. PMID 6811853.
- ^ Альтман Л.К. (11 мая 1982 г.). «Новое гомосексуальное расстройство беспокоит чиновников здравоохранения». Нью-Йорк Таймс. Получено 31 августа, 2011.
- ^ Гилман, Сандер L (1987). Гилман, Сандер Л. (ред.). «СПИД и сифилис: иконография болезней». Октябрь. 43: 87–107. Дои:10.2307/3397566. JSTOR 3397566.
- ^ «Продвигаться в адских обстоятельствах» (PDF). Американская ассоциация развития науки. 28 июля 2006 г.. Получено 23 июня, 2008.
- ^ Хер У (27 июля 1982 г.). «Имя чумы». Время. В архиве из оригинала 7 марта 2008 г.. Получено 10 марта, 2008.
- ^ Центры по контролю за заболеваниями (1982). «Последняя информация о синдроме приобретенного иммунодефицита (СПИД) - США». Еженедельный отчет о заболеваемости и смертности. 31 (37): 507–508, 513–514. PMID 6815471.
- ^ Галло Р.К., Зарин П.С., Гельманн Е.П., Роберт-Гурофф М., Ричардсон Э., Кальянараман В.С., Манн Д., Сидху Г.Д., Шталь Р.Э., Золла-Пазнер С., Лейбович Дж, Попович М. (1983). «Выделение вируса Т-клеточного лейкоза человека при синдроме приобретенного иммунодефицита (СПИД)». Наука. 220 (4599): 865–867. Bibcode:1983Научный ... 220..865Г. Дои:10.1126 / science.6601823. PMID 6601823.
- ^ Барре-Синусси Ф., Шерманн Дж. К., Рей Ф., Нугейр М. Т., Шамарэ С., Грюст Дж., Доге С., Акслер-Блин С., Везине-Брун Ф., Рузиу С., Розенбаум В., Монтанье Л. (1983). «Выделение Т-лимфотропного ретровируса от пациента с риском синдрома приобретенного иммунодефицита (СПИД)». Наука. 220 (4599): 868–871. Bibcode:1983Научный ... 220..868B. Дои:10.1126 / science.6189183. PMID 6189183. S2CID 390173.
- ^ «Нобелевская премия по физиологии и медицине 2008 года - пресс-релиз». www.nobelprize.org. Получено 28 января, 2018.
- ^ Крюдсон, Джон (30 мая 1991 г.). "ГАЛЛО ДОПУСКАЕТ ОБНАРУЖЕННЫЙ ФРАНЦУЗСКИЙ ВИРУС СПИДА". Чикаго Трибьюн. Получено 25 апреля, 2020.
- ^ Олдрич, Роберт; Уотерспун, Гарри, ред. (2001). Кто есть кто в истории геев и лесбиянок. Лондон: Рутледж. п. 154. ISBN 978-0-415-22974-6.
- ^ Levy JA; и другие. (1984). «Выделение лимфоцитопатических ретровирусов от больных СПИДом Сан-Франциско». Наука. 225 (4664): 840–842. Bibcode:1984Научный ... 225..840Л. Дои:10.1126 / science.6206563. PMID 6206563.
- ^ Леви Дж.А., Камински Л.С., Морроу В.Дж., Штаймер К., Люсиу П., Дина Д., Хокси Дж., Оширо Л. (1985). «Заражение ретровирусом, связанное с синдромом приобретенного иммунодефицита». Анналы внутренней медицины. 103 (5): 694–699. Дои:10.7326/0003-4819-103-5-694. PMID 2996401.
- ^ Sharp PM, Hahn BH (2011). «Истоки ВИЧ и пандемия СПИДа». Перспективы Колд-Спринг-Харбор в медицине. 1 (1): a006841. Дои:10.1101 / cshperspect.a006841. ЧВК 3234451. PMID 22229120.
- ^ Фариа Н.Р., Рамбаут А., Сушард М.А., Бэле Г., Бедфорд Т., Уорд М.Дж., Татем А.Дж., Соуза Д.Д., Аринаминпатия Н., Пепин Дж., Посада Д., Петерс М., Пибус О.Г., Лемей П. (2014). «Раннее распространение и вспышка эпидемии ВИЧ-1 в человеческих популяциях». Наука. 346 (6205): 56–61. Bibcode:2014Наука ... 346 ... 56F. Дои:10.1126 / science.1256739. ЧВК 4254776. PMID 25278604.
- ^ Гао Ф, Бэйлс Э., Робертсон Д.Л., Чен Й., Роденбург С.М., Майкл С.Ф., Камминс Л.Б., Артур Л.О., Петерс М., Шоу Г.М., Шарп П.М., Хан Б.Х. (1999). «Происхождение ВИЧ-1 у шимпанзе Pan troglodytes troglodytes». Природа. 397 (6718): 436–41. Bibcode:1999Натура.397..436Г. Дои:10.1038/17130. PMID 9989410. S2CID 4432185.
- ^ Кил Б.Ф., Ван Хеуверсвин Ф., Ли И, Бейлес Э, Такехиса Дж., Сантьяго М.Л., Биболлет-Руш Ф, Чен И, Уэйн Л.В., Льежуа Ф, Лоул С., Нголе Э.М., Бьенвеню Y, Делапорте Е, Брукфилд Дж. Ф., Шарп П.М. , Шоу Г.М., Питерс М., Хан Б.Х. (2006). «Шимпанзе - резервуары пандемического и непандемического ВИЧ-1». Наука. 313 (5786): 523–6. Bibcode:2006Научная ... 313..523K. Дои:10.1126 / science.1126531. ЧВК 2442710. PMID 16728595.
- ^ Гудье Дж. Л., Казазян Х. Х. (2008). «Ретротранспозоны снова: сдерживание и реабилитация паразитов». Клетка. 135 (1): 23–35. Дои:10.1016 / j.cell.2008.09.022. PMID 18854152. S2CID 3093360.
- ^ Sharp PM, Bailes E, Chaudhuri RR, Rodenburg CM, Santiago MO, Hahn BH (2001). «Истоки вирусов синдрома приобретенного иммунодефицита: где и когда?». Философские труды Королевского общества B. 356 (1410): 867–76. Дои:10.1098 / rstb.2001.0863. ЧВК 1088480. PMID 11405934.
- ^ Калиш М.Л., Вулф Н.Д., Ндонгмо С.Б., МакНичолл Дж., Роббинс К.Э., Аиду М., Фонджунго П.Н., Алемнджи Г., Зех К., Джоко К.Ф., Мпоуди-Нголе Э., Берк Д.С., Народ TM (2005). «Охотники из Центральной Африки, зараженные вирусом обезьяньего иммунодефицита». Возникающие инфекционные заболевания. 11 (12): 1928–30. Дои:10.3201 / eid1112.050394. ЧВК 3367631. PMID 16485481.
- ^ а б Маркс П.А., Алькабес П.Г., Друкер Э. (2001). «Серийный перенос вируса обезьяньего иммунодефицита через нестерильные инъекции и появление эпидемического вируса иммунодефицита человека в Африке». Философские труды Королевского общества B. 356 (1410): 911–20. Дои:10.1098 / rstb.2001.0867. ЧВК 1088484. PMID 11405938.
- ^ Worobey M, Gemmel M, Teuwen DE, Haselkorn T, Kunstman K, Bunce M, Muyembe JJ, Kabongo JM, Kalengayi RM, Van Marck E, Gilbert MT, Wolinsky SM (2008). «Прямое свидетельство широкого разнообразия ВИЧ-1 в Киншасе к 1960 году». Природа. 455 (7213): 661–4. Bibcode:2008 Натур.455..661Вт. Дои:10.1038 / природа07390. ЧВК 3682493. PMID 18833279.
- ^ а б де Соуза Дж. Д., Мюллер В., Лемей П., Вандамм А. М. (2010). Мартин Д.П. (ред.). «Высокая заболеваемость ГУД в начале 20 века создала особенно благоприятное временное окно для происхождения и начального распространения эпидемических штаммов ВИЧ». PLOS ONE. 5 (4): e9936. Bibcode:2010PLoSO ... 5.9936S. Дои:10.1371 / journal.pone.0009936. ЧВК 2848574. PMID 20376191.
- ^ Чжу Т., Корбер Б.Т., Нахмиас А.Дж., Хупер Э., Шарп П.М., Хо Д.Д. (1998). «Африканская последовательность ВИЧ-1 с 1959 года и последствия для происхождения эпидемии». Природа. 391 (6667): 594–7. Bibcode:1998Натура.391..594Z. Дои:10.1038/35400. PMID 9468138. S2CID 4416837.
- ^ Колата, Джина (28 октября 1987 г.). «Смерть мальчика в 1969 году предполагает, что СПИД несколько раз вторгался в США». Нью-Йорк Таймс. Получено 11 февраля, 2009.
- ^ Читнис А., Ролз Д., Мур Дж. (2000). «Происхождение ВИЧ типа 1 в колониальной французской экваториальной Африке?». Исследования СПИДа и ретровирусы человека. 16 (1): 5–8. Дои:10.1089/088922200309548. PMID 10628811. S2CID 17783758.
- ^ Дональд Макнил младший (16 сентября 2010 г.). «Предшественник ВИЧ был у обезьян на протяжении тысячелетий». Нью-Йорк Таймс. Получено 17 сентября, 2010.
Доктор Маркс считает, что решающим событием стало появление в Африке миллионов недорогих шприцев массового производства в 1950-х годах. ... подозреваю, что виноват рост колониальных городов. До 1910 года ни в одном центральноафриканском городе не проживало более 10 000 человек. Но городская миграция росла, увеличивая сексуальные контакты и приводя к кварталам красных фонарей.
дальнейшее чтение
- Берлиер В., Бурле Т., Лоуренс П., Хамзе Х., Ламберт С., Женин С., Веррие Б., Дьё-Ножан М.С., Поцетто Б., Делезе О. (2005). «Селективная секвестрация изолятов X4 эпителиальными клетками половых органов человека: значение для процесса отбора вирусного тропизма во время передачи ВИЧ половым путем». Журнал медицинской вирусологии. 77 (4): 465–74. Дои:10.1002 / jmv.20478. PMID 16254974. S2CID 25762969.
- Объединенная программа Организации Объединенных Наций по ВИЧ / СПИДу (ЮНЭЙДС) (2011 г.). Глобальные меры в ответ на ВИЧ / СПИД, обновление эпидемии и прогресс сектора здравоохранения в направлении всеобщего доступа (PDF). Объединенная программа Организации Объединенных Наций по ВИЧ / СПИДу.
- Мучичча Б, Падула Ф, Вичини Э, Гандини Л, Лензи А, Стефанини М (2005). «Бета-хемокиновые рецепторы 5 и 3 экспрессируются в области головы человеческого сперматозоида». Журнал FASEB. 19 (14): 2048–50. Дои:10.1096 / fj.05-3962fje. PMID 16174786. S2CID 7928126.


